 , 王学东1
, 王学东1
 , 李志涛2, 季冬雪1, 华珞1
, 李志涛2, 季冬雪1, 华珞11. 首都师范大学资源环境与旅游学院, 北京 100048;
2. 环境保护部环境规划院, 北京 100012
收稿日期: 2018-02-02; 修回日期: 2018-03-08; 录用日期: 2018-03-08
基金项目: 国家自然科学基金项目(No.41501537);北京市教育委员会科技计划项目(No.KM201610028012)
作者简介: 王祺鑫(1994-)女, E-mail:applexinge@163.com
通讯作者(责任作者): 王学东, E-mail:xdwang@cnu.edu.cn
摘要: 通过水培实验,研究了不同Mg2+浓度下Cu、Zn、Ni单独及Cu-Ni、Zn-Ni复合对小麦根的毒性并分别建立了3个元素的BLM.利用Cu、Zn、Ni单一毒性数据,计算了复合金属离子与生物配体结合数量指数(fmix),由此建立了用于预测Cu-Ni、Zn-Ni联合毒性的BLM-fmix模型.结果表明,溶液中Mg2+浓度增加,能够减弱单一Cu、Zn、Ni和Cu-Ni、Zn-Ni复合对小麦根的毒性.在复合体系中,Cu-Ni复合的TU50(对小麦根长产生50%抑制作用时的毒性单位值)分别为1.18、1.33、1.31,略大于1,表现为弱拮抗作用;而Zn-Ni复合的TU50分别为4.22、2.26、2.16,表现为强拮抗作用.BLM-fmix模型能够准确预测Cu-Ni、Zn-Ni联合作用下小麦根长,预测和实测值的相关系数及标准误差分别为0.94、8.87(Cu-Ni复合)和0.92、10.14(Zn-Ni复合),该结果为重金属复合污染土壤的评价和修复提供理论依据.
关键词:拓展生物配体模型重金属复合毒性小麦
Extended biotic ligand model for prediction of mixture toxicity of Cu-Ni, Zn-Ni to wheat effected by Mg
WANG Qixin1
 , WANG Xuedong1
, WANG Xuedong1
 , LI Zhitao2, JI Dongxue1, HUA Luo1
, LI Zhitao2, JI Dongxue1, HUA Luo1 1. College of Resource Environment and Tourism, Capital Normal University, Beijing 100048;
2. Chinese Academy for Environmental Planning, Beijing 100012
Received 2 February 2018; received in revised from 8 March 2018; accepted 8 March 2018
Supported by the National Natural Science Foundation of China (No.41501537) and the Beijing Municipal Commission of Education Foundation (No.KM201610028012)
Biography: WANG Qixin(1994—), female, E-mail:applexinge@163.com
*Corresponding author: WANG Xuedong, E-mail: xdwang@cnu.edu.cn
Abstract: Toxicity of Cu, Zn, Ni alone and Cu-Ni, Zn-Ni compounds to wheat were tested by water cultivation experiment under different concentrations of Mg2+, and BLM (biotic ligand model) of Cu, Zn and Ni were established respectively. Using data of single metal element (Cu, Zn and Ni) BLM combined with toxicity index, the overall amounts of metal ions bound to the biotic ligands (fmix) was calculateed. Furthermore, BLM- fmix was established to predict the joint toxicity of Cu-Ni and Zn-Ni. The results showed that the toxicity of single Cu, Zn and Ni as well as the combined toxicity of Cu-Ni, Zn-Ni were decreased with the increasing Mg2+ concentration. In the compound solution, the TU50 values (when the root length of wheat was inhibited by 50%) of Cu-Ni compound was 1.18, 1.33, 1.31, slightly greater than 1, which showed weak antagonism between Cu and Ni; Whereas in Zn-Ni composite system, the TU50 value was 4.22, 2.26, 2.16, which showed strong antagonistic effect. BLM-fmix could accurately predict the root length of wheat under the combined action of Cu-Ni and Zn-Ni. The correlation coefficient and standard error of the predicted and measured values were 0.94, 0.87 in Cu-Ni and 0.92, 10.14 in Zn-Ni respectively. The results provided a theoretical basis for the evaluation and remediation contaminated soils of heavy metal.
Key words: extended biotic ligand modelheavy metalstoxicitywheat
1 引言(Introduction)由于人类活动的影响, 大量的重金属如Cd、Cu、Ni和Zn等被释放到自然环境中(Charles et al., 2014).重金属含量的升高可能会对环境中的动植物产生负面影响, 并可能通过食物链或直接摄取等方式对人体健康造成损害.控制环境中重金属的风险需要评价其毒性, 目前的风险评价方法主要基于单一金属元素(Backhaus et al., 2012).然而, 重金属常以两种或多种复合的形式存在(Schmidt et al., 2010).因此, 建立一种预测重金属复合作用的评价方法对于环境风险的管理十分必要.
毒性单位(TU)法是一种常用的评估化学混合物毒性的模型(Chen et al., 2002).TU可以用公式表示为:
 | (1) |
目前, 一些研究者们正尝试使用单一元素BLM评价复合金属的毒性, 这样可以应用已有的数据来研究复合污染, 节省了实验时间和成本.如Playle等(2004)将BLM与TU法结合来解释复合金属对水生生物造成的毒性.Hatano等(2008)表明, 使用BLM模型得出的单一金属毒性数据来计算TU值, 可以用来估算Cu、Cd对浮萍的联合作用.Iwasaki等(2015)发现, 用基于TU法扩展的BLM, 可以通过与Ca2+摄取有关的生物配体量来预测Zn、Cu和Cd对虹鳟鱼的复合毒性.
过去更多的研究集中于水体环境, 对土壤中的研究较少, 但在水体中复合金属毒性的研究方法为其在土壤中的应用提供了借鉴(Wang et al., 2017; Wu et al., 2017; 陈潇霖等, 2016).土壤矿物、有机质等对金属形态和生物有效性影响较为复杂, 而土壤溶液环境与水体环境相似, 所以土壤中生物配体模型研究大多从土壤溶液做起.
基于此, 本文以Cu-Ni、Zn-Ni重金属元素二元复合作用下的生物毒性为切入点, 综合考虑阳离子对生物体的保护作用以及金属离子间的相互作用, 通过模拟土壤溶液试验, 在单一Cu、Zn、Ni毒性数据的基础上, 建立Cu-Ni、Zn-Ni复合对小麦联合毒性的拓展BLM, 从而为重金属联合毒性风险评价提供依据.
2 材料与方法(Materials and methods)2.1 试验设计2.1.1 Cu、Zn、Ni单一元素对小麦的毒性采用模拟土壤溶液进行水培实验, 通过小麦相对根长测试来评估Cu、Zn、Ni单一作用下对小麦急性毒性的影响.利用单因素控制变量的方法研究不同浓度的Mg2+分别对小麦Cu、Zn、Ni急性毒性的影响.Mg2+浓度设置为0.05、0.5、2 mmol·L-1.每组浓度Mg2+分别与8个不同浓度的Cu、Zn、Ni进行交互实验.
Cu、Zn、Ni的浓度设置范围保证对生物从无毒到完全毒性.其中, Cu浓度分别为0、0.2、0.4、0.8、1.6、3.2、6.4、12.8 μmol·L-1;Zn浓度分别为0、10、20、40、80、160、320、630 μmol·L-1;Ni浓度分别为0、2、4、8、16、32、64、128 μmol·L-1.受试液中其余各离子浓度的变化范围参照自然土壤孔隙水的离子浓度范围(Kandegedara et al., 1999), 即0.2 mmol·L-1 Ca、2.5 mmol·L-1 Na、0.08 mmol·L-1 K, pH值调节为6.0±0.1.以上浓度均为设计浓度, 每个处理设置3个重复.
2.1.2 Cu-Ni、Zn-Ni二元复合对小麦的联合毒性依据单一金属元素对小麦急性毒性的测试结果, 分别对Cu-Ni、Zn-Ni复合体系按1:1毒性比设置复合浓度, 每种复合设置7个浓度梯度, l组空白对照.每组复合处理下单独变化Mg2+浓度分别与不同浓度梯度的Cu-Ni、Zn-Ni复合进行交互实验.具体设置见表 1.受试液中其余各离子浓度的变化范围以及pH值同单一元素设置.每个处理3个重复.
表 1(Table 1)
| 表 1 二元复合体系的质量浓度配比 Table 1 Mass concentration ratio of binary composite system | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
表 1 二元复合体系的质量浓度配比 Table 1 Mass concentration ratio of binary composite system
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2.2 溶液配制在去离子水中加入不同体积的CaCl2、MgSO4、NaCl和KCl制备基础培养液, Ca2+、Mg2+、Na+和K+的浓度参照Wang等(2017)设置.所有处理溶液的pH调节为6.0, pH调节采用1 mol·L-1 2-(N-吗啡啉)乙磺酸(MES, 2-[N-morpholino] ethane sulfonic acid)与1 mol·L-1 NaOH或1 mol·L-1 HCl((Wang et al., 2010).所使用的化学物质均为分析或优级纯, 溶液为去离子水.溶液配制完成后稳定24 h使用.
2.3 毒性测试根长抑制实验参照USEPA(1996)和ISO11269-1的方法(罗小三等, 2007), 小麦种子用10%的双氧水溶液消毒洗净后置于去离子水湿润的滤纸上, 然后放于培养箱发芽, 培养箱温度保持(20±1) ℃, 无光照.24 h后选取发芽一致种子置于350 mL培养杯中开始根伸长抑制实验.每个培养杯放置6颗种子, 每个处理设置3个重复, 所有培养杯随机放置于气候箱中培养, 每天保持12~14 h光照, 温度为(20±2)℃;8~12 h黑暗, 温度为(18±2)℃.光照强度为25000 lux, 每隔1 d更换1次溶液, 培养4 d后测定根长.
2.4 数据统计和处理重溶液中金属形态采用WHAM6.0软件估计, 输入温度, 溶液中H+、Cu2+、Zn2+、Ni2+、Ca2+、Na+、K+、Mg2+的浓度和pH值.考虑到试验处于开放系统, CO2的分压设为35 Pa.
小麦相对净根长(RNE)的计算如公式(2)所示.
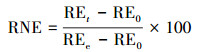 | (2) |
与重金属浓度剂量效应关系采用log-logistic拟合(公式(3)), 利用公式(3)能够根据重金属Cu、Zn、Ni的浓度以及相应小麦相对净根长(RNE), 拟合出EC50值(小麦根长受到50%抑制时的金属离子浓度或活度).
 | (3) |
2.5 参数估计方法BLM中假设金属与BLS的相互作用是竞争关系, 以金属离子结合的生物配体数占配体总数的比值f作为判断金属毒性的关键指标(Jho et al., 2011).
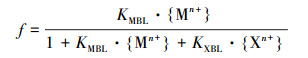 | (4) |
重金属离子对小麦的毒性指标f与小麦相对净根长采用logistic曲线拟合(Thakali et al., 2006a)(公式(5)), 由此可拟合复合金属与小麦根长的剂量效应关系.
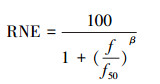 | (5) |
复合金属的毒性可由TUf值和fmix值来表示, TUf值的计算如方程(6)所示.其中考虑了阳离子与金属离子之间的竞争.然而, TUf值无法表示复合物中金属离子之间的相互竞争, 因为在TUf值中, 金属离子被认为作用在生物体表面的不同位点上, 复合物的TUf值由每种重金属的TUf值相加得到.
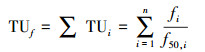 | (6) |
 | (7) |
3 结果与分析(Results and analysis)3.1 单一金属Cu、Zn、Ni对小麦的毒性及其BLM模型不同Mg浓度下小麦相对净根长与溶液中自由Cu2+、Zn2+、Ni2+活度的剂量-反应关系如图 1所示.由图可见, 随着Mg浓度的增高, Cu、Zn、Ni单独作用于小麦的剂量效应曲线均逐渐向右偏移, 这表明在实验浓度范围内Mg浓度的增加可以减弱Cu、Zn、Ni单独作用时对小麦的毒性.根据公式(3), 计算了不同Mg浓度下Cu、Zn、Ni对小麦毒性的EC50值(表 2).由表可见, Mg浓度从0.05 mmol·L-1增加到2 mmol·L-1, EC50(Cu2+)由0.50 μmol·L-1升高至0.89 μmol·L-1;EC50(Zn2+)由81.86 μmol·L-1升高至297.57 μmol·L-1, 提高了3.6倍;EC50(Ni2+)由6.21 μmol·L-1升高至25.33 μmol·L-1, 提高了4倍.由此可见, 一定浓度范围内, Mg能够缓减Cu、Zn、Ni对小麦的毒性.类似的结果在以往的研究中也有报道, 如Lock等(2007a)通过水培方式研究发现Mg2+活度的增加能够使Cu2+对大麦根长半数抑制浓度提高两倍.Mg2+不仅能够减轻重金属对植物的毒害, 还可以抑制多种重金属对动物的危害, De Schamphelaere等(2004)发现Mg2+浓度的增加导致Zn2+对虹鳟鱼的毒性降低, 同样Mg2+能够降低蚯蚓对Cd的吸收, 从而降低其致死率(Li et al., 2009).
图 1(Fig. 1)
 |
| 图 1 不同Mg浓度下RNE与Cu2+、Zn2+、Ni2+之间的剂量效应关系 Fig. 1Dose-response relationship between RNE and Cu2+、Zn2+and Ni2+ under different magnesium concentrations |
表 2(Table 2)
| 表 2 不同Mg浓度下单一重金属元素对小麦根长的EC50 Table 2 EC50 of wheat roots with the action of single heavy metals under different magnesium concentrations | ||||||||||||||||
表 2 不同Mg浓度下单一重金属元素对小麦根长的EC50 Table 2 EC50 of wheat roots with the action of single heavy metals under different magnesium concentrations
| ||||||||||||||||
利用Mg2+与Cu2+、Zn2+、Ni2+竞争结果, 结合公式(5)分别建立3种元素的BLM, 模型的拟合参数如表 3所示.由表可见Cu、Zn、Ni与小麦根配体的络合常数(logK)分别为6.15、3.94、4.86, 这表明Cu的毒性最大, Zn的毒性最小, 和前人的研究结果相似.Wang等(2017)研究了Cu、Zn与小麦的络合常数, 得出的结果为logKCu=5.87, logKZn=4.06;Wu等(2017)的研究表明Cu的络合常数为5.94.目前还未发现Ni与小麦的logK值报道, Lock等(2007c)研究了Ni对大麦的毒性, 得出的logK值为5.27, 与本文结果也大致相似.Mg的logK值在2.84~3.40之间, 这反映了Mg与小麦根配体结合能力远小于Cu、Zn、Ni, 但一般土壤中Mg的含量远高于重金属元素, 所以常会表现出一定的竞争作用.
表 3(Table 3)
| 表 3 单一重金属作用下BLM模型的拟合参数 Table 3 Fitting parameters of BLM model under the action of single heavy metal | |||||||||||||||||||||||||
表 3 单一重金属作用下BLM模型的拟合参数 Table 3 Fitting parameters of BLM model under the action of single heavy metal
| |||||||||||||||||||||||||
3.2 Cu-Ni、Zn-Ni二元复合对小麦的联合毒性根据公式(1)计算了不同Mg梯度下单一元素及二元复合金属的TU值, 并绘制了TU与RNE的剂量效应关系图(图 2).由图 2可见, 对于Cu-Ni复合体系, 无论何种Mg浓度下, Cu-Ni复合较其单独作用下的剂量效应曲线均略向右偏移.按照TU模型理论, 剂量效应曲线偏移表示复合体系中金属离子间存在着拮抗或者协同作用, 不发生偏移为加和作用.由此推断本研究中Cu-Ni复合对小麦产生的毒性具有弱拮抗作用.对于Zn-Ni复合体系, 3个Mg浓度下二者联合作用的剂量效应曲线较Zn、Ni单一曲线明显向右偏移, 表明Zn-Ni复合呈现出明显的拮抗作用.为进一步验证二元复合金属的作用, 计算了不同Mg浓度下复合体系中的TU50值.在Cu-Ni复合中, 3个Mg浓度下的TU50分别为1.18、1.33、1.31.在Zn-Ni复合中, 3个Mg浓度下的TU50分别为4.22、2.26、2.16.根据TU模型理论, 当TU>1为拮抗作用, 因此Cu-Ni呈现出弱拮抗作用, 而Zn-Ni较Cu-Ni的拮抗作用更强.钟旭(2015)利用浓度加和模型和效应加和模型研究了Cu-Ni对大麦的联合作用, 也发现低剂量Ni对Cu具有明显的拮抗作用, 这和本研究结果相似.
图 2(Fig. 2)
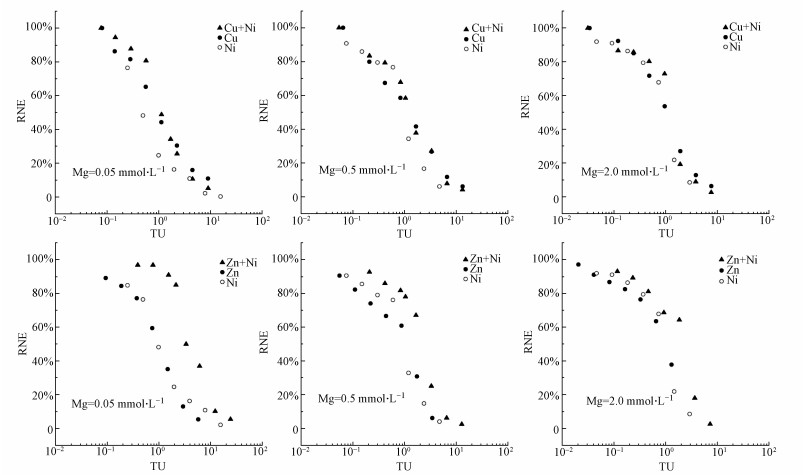 |
| 图 2 不同Mg2+浓度下RNE与Cu-Ni、Zn-Ni复合体系下TU值的剂量效应关系 Fig. 2The dose-effect relationship between RNE and TU values in Cu-Ni and Zn-Ni composite system under different concentrations of Mg2+ |
Cu-Ni、Zn-Ni的拮抗作用可能与其化学性质的相似性有关, 有研究报道金属离子对水生生物的毒性与其理化性质如金属离子软指数、共价常数等指标具有较好的相关关系(Wu et al., 2013).本研究的3个金属元素Cu、Zn、Ni的多个理化性质指标相似, 如软指数(Cu 0.10、Zn 0.11、Ni 0.13)、共价半径(Cu 2.64、Zn 2.02、Ni 2.52)、极化力参数(Cu 5.48、Zn 5.41、Ni 5.80)等, 因此, 共同的性质导致它们与生物体具有相似的作用方式, 从而产生拮抗作用.本研究没有探讨Cu-Zn的复合作用, 但已有研究报道Cu-Zn在低Ca2+浓度下的水配溶液中以及在土壤介质中对大麦的毒性也表现出拮抗作用(Versieren et al., 2014; Qiu et al., 2016).Zn-Ni拮抗作用远较Cu-Ni作用强可能和它们与小麦根配体的络合常数有关, Zn、Ni的logK较Cu、Ni更相近, 因此竞争作用更强烈.
3.3 Cu-Zn、Zn-Ni联合毒性的预测模型根据公式(6), 考虑了陪伴离子(Mg2+)的竞争, 计算了TUf值, 然后利用TUf值拟合RNE(公式(5)), 建立了BLM-TUf模型.当同时考虑Mg2+和金属离子之间的拮抗作用时, 根据公式(7)计算了fmix值, 同理利用fmix拟合RNE, 建立了BLM-fmix模型, 如图 3所示.结果显示, 不论是Cu-Ni还是Zn-Ni复合体系, 考虑了金属离子之间拮抗的BLM-fmix模型能够更为准确的预测其对小麦的毒性, 利用BLM-fmix预测值与实测值之间的可决系数(R2)和根均方差(RMSE)分别为:0.94、8.87(Cu-Ni);0.92、10.14(Zn-Ni).而不考虑金属离子之间拮抗的BLM-TUf模型中, R2和RMSE分别为:0.89、11.66(Cu-Ni);0.34、29.30(Zn-Ni), 其预测复合物毒性的准确性明显低于BLM-fmix的结果.这也进一步证实了Cu-Ni、Zn-Ni具有拮抗作用的现象.
图 3(Fig. 3)
 |
| 图 3 基于BLM-fmix模型的Cu-Ni、Zn-Ni对小麦联合毒性的剂量效应曲线 Fig. 3Dose-effect curve of combined toxicity of Cu-Ni and Zn-Ni to wheat based on BLM-fmix model |
上述结果表明, BLM-fmix能够较为准确预测Cu-Zn、Zn-Ni的联合毒性, 这在以往的研究中也得到了证实(Jho et al., 2011; Qiu et al., 2015).这些研究也表明, 当金属离子之间呈现拮抗作用时, BLM-fmix模型更具优势, 但当金属离子之间呈其他作用方式时预测效果则降低.例如Liu等(2014)的研究表明用BLM-fmix预测Cu-Ni对于莴苣毒性的效果不太理想(R2=0.58, RMSE=18.47), 这可能和金属元素复合的浓度配比、植物种类等有关.所以针对复合金属的毒性预测模型需要我们进行更深入的研究, 以便更好地了解金属之间相互作用的机制, 从而建立更加普适的重金属联合作用评价模型.
4 结论(Conclusions)1) 增加水培溶液中Mg2+活度可以减轻Cu、Zn、Ni对小麦根伸长的毒性作用, Mg浓度从0.05 mmol·L-1增加到2 mmol·L-1分别使EC50(Cu2+)提高1.78倍、EC50(Zn2+)提高3.6倍、EC50(Ni2+)提高4倍;考虑Mg竞争后建立单一元素BLM, 拟合得到Cu、Zn、Ni与配体的的络合常数分别为logKCu=6.15, logKZn=3.94, logKNi=4.86.
2) 3组Mg浓度下, Cu-Ni、Zn-Ni复合对小麦根毒性均表现为拮抗作用, Cu-Ni复合对小麦根伸长的TU50值在1.18~1.31之间, 表现为弱拮抗作用;而Zn-Ni复合下的TU50值在2.26~4.22之间, 表现为强拮抗作用.
3) 基于单一金属Cu、Zn、Ni的BLM毒性数据, 结合fmix指数, 建立了BLM-fmix模型并预测了Cu-Ni、Zn-Ni二元复合对小麦的毒性作用, 结果表明BLM-fmix模型能够较好地预测Cu-Ni、Zn-Ni复合体系对小麦根伸长的毒性, 预测和实测偏差可控制在10%, 是一种很有前景的模型.
参考文献
| Altenburger R, Backhaus T, Boedeker W, et al. 2000. Predictability of the toxicity of multiple chemical mixtures to Vibrio fischeri:Mixtures composed of similarly acting chemicals[J]. Environmental Toxicology and Chemistry, 19(9): 2341–2347.DOI:10.1897/1551-5028(2000)019<2341:POTTOM>2.3.CO;2 |
| Backhaus T, Faust M. 2012. Predictive environmental risk assessment of chemical mixtures:A conceptual framework[J]. Environmental Science & Technology, 46(5): 2564–2573. |
| Charles J, Crini G, Degiorgi F, et al. 2014. Unexpected toxic interactions in the freshwater amphipod Gammarus pulex (L.) exposed to binary copper and nickel mixtures[J]. Environmental Science and Pollution Research, 21(2): 1099–1111.DOI:10.1007/s11356-013-1978-1 |
| Chen C Y, Lu C L. 2002. An analysis of the combined effects of organic toxicants[J]. Science of the Total Environment, 289(1/3): 123–132. |
| 陈潇霖, 王学东, 田雨, 等. 2016. 铜、锌对小麦的联合毒性及其预测模型研究[J]. 环境科学学报, 2016, 36(4): 1493–1499. |
| Clifford M, Mcgeer J C. 2010. Development of a biotic ligand model to predict the acute toxicity of cadmium to Daphnia pulex[J]. Aquatic Toxicology, 98(1): 1–7. |
| De Schamphelaere K a C, Janssen C R. 2004. Bioavailability and chronic toxicity of zinc to juvenile rainbow trout (Oncorhynchus mykiss):Comparison with other fish species and development of a biotic ligand model[J]. Environmental Science & Technology, 38(23): 6201–6209. |
| Hatano A, Shoji R. 2008. Toxicity of copper and cadmium in combinations to duckweed analyzed by the biotic ligand model[J]. Environmental Toxicology, 23(3): 372–378.DOI:10.1002/(ISSN)1522-7278 |
| Iwasaki Y, Kamo M, Narro W. 2015. Testing an application of a biotic ligand model to predict acute toxicity of metal mixtures to rainbow trout[J]. Environmental Toxicology and Chemistry, 34(4): 754–760.DOI:10.1002/etc.v34.4 |
| Jho E H, An J, Nam K. 2011. Extended biotic ligand model for prediction of mixture toxicity of Cd and Pb using single metal toxicity data[J]. Environmental Toxicology and Chemistry, 30(7): 1697–1703.DOI:10.1002/etc.v30.7 |
| Jiang Y, Gu X Y, Zhu B J, et al. 2017. Development and validation of abiotic ligand model for nickel toxicity to wheat (Triticum aestivum)[J]. Journal of Environmental Sciences, 62: 22–30.DOI:10.1016/j.jes.2017.06.005 |
| Kandegedara A, Rorabacher D B. 1999. Noncomplexing tertiary amines as "better" buffers covering the range of ph 3-11.Temperature dependence of their acid dissociation constants[J]. Analytical Chemistry, 71(15): 3140–3144.DOI:10.1021/ac9902594 |
| Le T T Y, Peijnenburg W J G M, Hendriks A J, et al. 2012. Predicting effects of cations on copper toxicity to lettuce (Lactuca sativa) by the biotic ligand model[J]. Environmental Toxicology and Chemistry, 31(2): 355–359.DOI:10.1002/etc.v31.2 |
| 李波, 马义兵, 王学东. 2014. 我国土壤中重金属铜的生物配体模型的建立与应用[J]. 生态毒理学报, 2014, 9(4): 632–639. |
| Li L Z, Zhou D M, Wang P, et al. 2009. Effect of cation competition on cadmium uptake from solution by the earthworm Eisenia Fetida[J]. Environmental Toxicology and Chemistry, 28(8): 1732–1738.DOI:10.1897/09-001.1 |
| 李晓敏, 胡莹, 黄益宗, 等. 2017. 应用生物配体模型研究阳离子及pH值对水稻锌毒性的影响[J]. 环境化学, 2017, 36(8): 1724–1734.DOI:10.7524/j.issn.0254-6108.2017032005 |
| Liu Y, Vijver M G, Peijnenburg W. 2014. Comparing three approaches in extending biotic ligand models to predict the toxicity of binary metal mixtures (Cu-Ni, Cu-Zn and Cu-Ag) to lettuce (Lactuca sativa L.)[J]. Chemosphere, 112: 282–288.DOI:10.1016/j.chemosphere.2014.04.077 |
| Lock K, Criel P, De Schamphelaere K a C, et al. 2007a. Influence of calcium, magnesium, sodium, potassium and ph on copper toxicity to barley (Hordeum vulgare)[J]. Ecotoxicology and Environmental Safety, 68(2): 299–304.DOI:10.1016/j.ecoenv.2006.11.014 |
| Lock K, De Schamphelaere K a C, Becaus S, et al. 2007b. Development and validation of a terrestrial biotic ligand model predicting the effect of cobalt on root growth of barley (Hordeum vulgare)[J]. Environmental Pollution, 147(3): 626–633.DOI:10.1016/j.envpol.2006.10.003 |
| Lock K, Van Eeckhout H, De Schamphelaere K a C, et al. 2007c. Development of a biotic ligand model (blm) predicting nickel toxicity to barley (Hordeum vulgare)[J]. Chemosphere, 66(7): 1346–1352.DOI:10.1016/j.chemosphere.2006.07.008 |
| 罗小三, 李连祯, 周东美. 2007. 陆地生物配体模型(t-blm)初探:镁离子降低铜离子对小麦根的毒性[J]. 生态毒理学报, 2007, 2(1): 41–48. |
| Niyogi S, Wood C M. 2004. Biotic ligand model, a flexible tool for developing site-specific water quality guidelines for metals[J]. Environmental Science & Technology, 38(23): 6177–6192. |
| Norwood W P, Borgmann U, Dixon D G. 2007. Chronic toxicity of arsenic, cobalt, chromium and manganese to Hyalella azteca in relation to exposure and bioaccumulation[J]. Environmental Pollution, 147(1): 262–272.DOI:10.1016/j.envpol.2006.07.017 |
| Playle R C. 2004. Using multiple metal-gill binding models and the toxic unit concept to help reconcile multiple-metal toxicity results[J]. Aquatic Toxicology, 67(4): 359–370.DOI:10.1016/j.aquatox.2004.01.017 |
| Qiu H, Vijver M G, He E K, et al. 2015. Incorporating bioavailability into toxicity assessment of Cu-Ni, Cu-Cd, and Ni-Cd mixtures with the extended biotic ligand model and the WHAM-Ftox approach[J]. Environmental Science and Pollution Research, 22(23): 19213–19223.DOI:10.1007/s11356-015-5130-2 |
| Qiu H, Versieren L, Rangel G G, et al. 2016. Interactions and toxicity of Cu-Zn mixtures to Hordeum vulgare in different soils can be rationalized with bioavailability-based prediction models[J]. Environmental Science & Technology, 50(2): 1014–1022. |
| Schmidt T S, Clements W H, Mitchell K A, et al. 2010. Development of a new toxic-unit model for the bioassessment of metals in streams[J]. Environmental Toxicology and Chemistry, 29(11): 2432–2442.DOI:10.1002/etc.v29:11 |
| Song N N, Zhong X, Li B, et al. 2014. Development of a multi-species biotic ligand model predicting the toxicity of trivalent chromium to barley root elongation in solution culture[J]. Plos One, 9(8): e105174.DOI:10.1371/journal.pone.0105174 |
| Thakali S, Allen H E, Di Toro D M, et al. 2006a. A terrestrial biotic ligand model.1. Development and application to Cu and Ni toxicities to barley root elongation in soils[J]. Environmental Science & Technology, 40(22): 7085–7093. |
| Thakali S, Allen H E, Di Toro D M, et al. 2006b. A terrestrial biotic ligand model.2. application to Ni and Cu toxicities to plants, invertebrates and microbes in soil[J]. Environmental Science and Technology, 40(22): 7094–7100.DOI:10.1021/es061173c |
| Versieren L, Smets E, De Schamphelaere K, et al. 2014. Mixture toxicity of copper and zinc to barley at low level effects can be described by the biotic ligand model[J]. Plant and Soil, 381(1/2): 131–142. |
| Wang X D, Ji D X, Chen X L, et al. 2017. Extended biotic ligand model for predicting combined Cu-Zn toxicity to wheat (Triticum aestivum L.):Incorporating the effects of concentration ratio, major cations and pH[J]. Environmental Pollution, 230: 210–217.DOI:10.1016/j.envpol.2017.06.037 |
| 王学东, 马义兵, 华珞, 等. 2008. 铜对大麦(Hordeum vulgare)的急性毒性预测模型-生物配体模型[J]. 环境科学学报, 2008, 28(8): 1704–1712. |
| Wu F C, Mu Y S, Chang H, et al. 2013. Predicting water quality criteria for protecting aquatic life from physicochemical properties of metals or metalloids[J]. Environmental Science & Technology, 47(1): 446–453. |
| Wu M Y, Wang X D, Jia Z G, et al. 2017. Modeling acute toxicity of metal mixtures to wheat (Triticum aestivum L.) using the biotic ligand model-based toxic units method[J]. Scientific Reports, 7: 9443.DOI:10.1038/s41598-017-09940-5 |
| 郑琰, 顾雪元, 姜洋, 等. 2017. 3种毒性预测模型在镉对小麦根毒性预测中的应用及比较[J]. 生态毒理学报, 2017, 12(1): 173–183. |
| 钟旭. 2015. 铜镍对大麦的联合毒性研究[D]. 北京: 首都师范大学资源环境与旅游学院. 18-24 |
