 , 范儒1,2, 王敏琛1,2, 周靖祎1,2, 熊国华1,2,3, 王东启1,2
, 范儒1,2, 王敏琛1,2, 周靖祎1,2, 熊国华1,2,3, 王东启1,2

1. 华东师范大学GIS教育部重点实验室, 上海 200241;
2. 华东师范大学地球科学学部地理科学学院, 上海 200241;
3. 上海市青浦区环保局, 上海 201700
收稿日期: 2017-07-18; 修回日期: 2017-08-11; 录用日期: 2017-08-11
基金项目: 国家自然科学基金(No.41671467,41473094);科技基础性工作专项(No.2014FY210600);上海市青浦区环保局招标项目(No.SHXM-00-20160920-1641116331401);国家自然科学基金人才培养项目(No.J1310028)
作者简介: 吴佳栩(1996-), 女, E-mail: mushwu@163.com
通讯作者(责任作者): 王东启, E-mail: dqwang@geo.ecnu.edu.cn
摘要: 于2016年5月和7月,使用乙炔抑制法对淀山湖湖区13个样点表层6 cm原状沉积物反硝化速率进行了测定.结果表明,淀山湖表层沉积物中的反硝化速率具有显著的时空变化特征,变化范围在5.72~65.82 μmol·m-2·h-1之间,,春季反硝化速率为(28.52±26.21)μmol·m-2·h-1,夏季反硝化速率为(29.31±17.11)μmol·m-2·h-1.在空间上,表层0~3 cm沉积物中反硝化速率((17.91±11.80)μmol·m-2·h-1)高于下层3~6 cm沉积物反硝化速率((11.02±10.40)μmol·m-2·h-1);反硝化速率与沉积物中可提取NH4+-N含量成显著正相关(p < 0.05),耦合的硝化-反硝化过程是沉积物反硝化作用的主要机制.淀山湖湖区上半年通过反硝化作用可去除约278.70 t的氮,对控制水体氮浓度和削减氮负荷具有重要意义.
关键词:淀山湖沉积物反硝化速率乙炔抑制法
Denitrification ability of surficial sediments in Dianshan Lake and its environmental implications
WU Jiaxu1,2
 , FAN Ru1,2, WANG Minchen1,2, ZHOU Jingyi1,2, XIONG Guohua1,2,3, WANG Dongqi1,2
, FAN Ru1,2, WANG Minchen1,2, ZHOU Jingyi1,2, XIONG Guohua1,2,3, WANG Dongqi1,2

1. GIS Key Laboratory of Ministry of Education, East China Normal University, Shanghai 200241;
2. School of Geographical Science, East China Normal University, Shanghai 200241;
3. Qingpu District Environmental Protection Bureau of Shanghai, Shanghai 201700
Received 18 July 2017; received in revised from 11 August 2017; accepted 11 August 2017
Supported by the National Natural Science Foundation of China(No.41671467, 41473094), the Special Project of the Ministry of Science and Technology(No.2014FY210600), the Foundation of the Environmental Protection Agency of Shanghai Qingpu District (No.SHXM-00-20160920-1641116331401) and the National Natural Science Foundation of China(No.J1310028)
Biography: WU Jiaxu(1996—), female, E-mail: mushwu@163.com
*Corresponding author: WANG Dongqi, E-mail: dqwang@geo.ecnu.edu.cn
Abstract: In May and July 2016, sediment samples collected from 13 sampling sites in Dianshan Lake were analyzed for their denitrification rates by the acetylene inhibition method. The result shows that the denitrification rates of the 6 cm undisturbed soil vary from 5.72~65.82 μmol·m-2·h-1 with a significant spatiotemporal deviation. The denitrification rate in spring is (28.52±26.21) μmol·m-2·h-1 and the denitrification rate in summer is (29.31±17.11) μmol·m-2·h-1. On the spatial scale, the denitrification rate in the 0~3 cm layer ((17.91±11.80) μmol·m-2·h-1) was higher than that in the 3~6 cm layer ((11.02±10.40) μmol ·m-2·h-1); NH4+-N content is significant positively correlated with the denitrification rate and coupled Nitrification-denitrification is the main mechanism. Based on the research data, it is estimated that the first half year of the lake area can remove about 278.70 t N by denitrification, which is of great significance to control the nitrogen concentration level and reduce the nitrogen load of water body.
Key words: Dianshan Lakesedimentdenitrification rateacetylene inhibition method
1 引言(Introduction)随着化学肥料使用量的增加及生活污水的直接排放, 湖泊生态系统的污染日趋严重.目前我国有66%以上的湖泊、水库处于富营养化的水平(吴雅丽等, 2014), 其中, 随颗粒物沉降的有机质、氮、磷等污染物不断沉积在湖泊底泥中, 使沉积物污染成为水生生态系统恢复和管理中的常见问题(Zhong et al., 2010).研究表明, 在外源输入得到有效控制后, 沉积物可能作为氮元素的“源”, 成为湖泊水体氮营养盐重要的来源之一, 对水体的营养水平有着不可忽视的影响(Lawrence et al., 1965; Sundby et al., 1992).反硝化过程是地球生物氮循环的重要环节, 它是指土壤微生物在缺氧条件下, 利用硝酸盐为电子受体, 将无机氮还原为气态N2和N2O的过程(徐继荣等, 2004).与上覆水体相比, 沉积物往往处于缺氧环境, 因而是反硝化发生的主要场所(孙志高等, 2010).沉积物反硝化需要的硝酸盐既可来自上覆水, 即非耦合硝化-反硝化作用, 也可来自沉积物中NH4+经过硝化作用生成的硝酸盐, 即耦合硝化-反硝化作用(Risgaard et al., 1994).反硝化速率受温度、有机质含量、硝酸盐浓度、DO浓度、水体pH值、生物作用、氧化还原条件等因素影响较大.何岩等(2012)认为, 在水体治理中忽略沉积物反硝化脱氮过程会导致总氮去除率偏低.目前, 国内外常用的测定反硝化速率的方法包括乙炔抑制法、N2通量法、质量平衡法和同位素法等(Groffman et al., 2006).Berelson等(1998)测得Port Phillip海湾沉积物通过反硝化作用去除的氮盐约占整个水体氮的63%.太湖梅梁湾北部河口区内耦合硝化-反硝化占脱氮速率的比值约为39.53%, 开敞湖区为69.96%(徐辉等, 2009).美国Okeechobee湖由反硝化作用清除的氮比值约为9%~23%(Messer et al., 1983).据估计, 沉积物-水界面上的反硝化作用可去除湖泊外源性氮输入负荷的30%~50%(Seitzinger et al., 1980).因此, 反硝化作用是削减湖泊氮负荷, 降低水体富营养化程度最有效的途径(杨龙元等, 1998).
淀山湖作为上海市重要的水源地, 目前的研究方向主要集中于浮游植物对水质的影响, 对沉积物的研究较少.程曦等(2008)对淀山湖1986—2004年的观测数据进行分析, 认为淀山湖在20年间由中度富营养化转化为重度富营养化, 且1999年后水体氮、磷营养物大量聚集.卢嘉等(2010)分析了淀山湖2008年总氮的时空分布, 发现春、冬季总氮的质量浓度要明显高于夏、秋季.淀山湖水体的总氮多在1~4 mg·L-1的范围内变化(杨虹, 2010), 从表层沉积物来看, 在空间分布上西北部样点氮含量高, 东南部样点氮含量低, (康丽娟, 2012).基于此, 本文通过研究淀山湖沉积物的反硝化脱氮能力, 分析比较沉积物反硝化速率的时空变化特征及沉积物理化性质的影响, 以期为淀山湖的污染治理提供可靠的理论基础.
2 材料与方法(Materials and methods)2.1 研究区概况淀山湖(31°04'N~31°12'N, 120°54'E~121°01'E)位于上海市青浦区与江苏省昆山市、吴江市交界处, 属于亚热带季风气候, 四季分明, 日照充足, 雨量充沛, 年均温18.8 ℃.湖区面积62 km2, 平均水深2.1 m, 最大处水深3.6 m(杨龙元等, 1998).淀山湖地处长三角经济开发区, 是黄浦江上游重点水源保护区之一.由于该区域人口众多, 产业发达, 排污能力受到一定影响, 富营养化严重.1985年淀山湖湖区首次暴发蓝藻水华(康丽娟, 2012), 此后经过有关部门治理, 富营养化程度有所降低, 但对于湖区仍有隐患, 甚至影响到上海市饮用水和整体水环境的安全.
淀山湖总体呈东北-西南走向, 南窄北宽, 呈葫芦状(康丽娟, 2012), 西面为主要进水河道分布区, 东面为主要出水河道分布区.本次研究分别于2016年5月和7月在淀山湖采集春、夏两季的沉积物柱状样品.考虑到湖泊中部区域水质较均匀, 进出水口区域变化较复杂的特点, 在湖区的环湖周围共设置13个采样点(图 1).
图 1(Fig. 1)
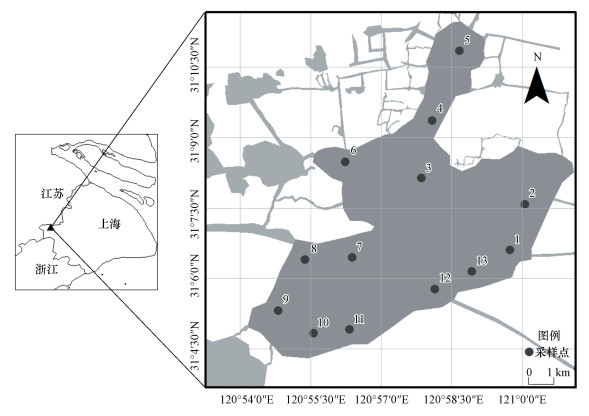 |
| 图 1 采样点分布示意图 Fig. 1Distribution map of sampling sites |
2.2 野外采样和室内培养于2016年5月、7月采集春、夏两季淀山湖底泥样品.使用抓斗采泥器, 在每个采样点采集沉积物样品和上覆水体样品, 在实验室水箱里建立和恢复沉积物水界面后, 采集3个平行柱样, 柱样采样器内置长24 cm、内径3.4 cm的有机玻璃管.原位柱样采集后, 将有机玻璃管取出, 直接进行培养, 尽量减少对柱样的扰动.每个柱样获得6~7 cm的沉积物样品.采集后的柱样两端使用螺口盖密封、直立放置送回实验室.
对于反硝化速率的测量采用乙炔抑制法.乙炔抑制法利用一定浓度的乙炔能抑制N2O还原为N2, NH4+氧化为N2O的原理, 根据N2O的产量来计算反硝化的速率.基于该法, 静置柱样使沉积物稳定后, 分上、下层各取3 cm左右土样于细口瓶中, 用橡胶塞封口.将细口瓶内抽真空并充满氮气, 使用注射器向瓶内注入10 mL纯净水和浓度为10%的乙炔, 培养2 h, 培养过程中每隔20 min摇晃细口瓶以保证反应充分进行.培养结束后, 使用带有气密性三通阀的注射器在每瓶中抽取10 mL样品, 并密封保存, 以待上机测试.测定使用的Agilent 7890Ⅱ气相色谱仪, 配置ECD检测器, 工作温度为330 ℃, 前置柱和分析柱参数分别为SS-1 m×2 mm×porapakQ(80/100)和SS-3 m×2 mm×porapakQ(80/100), 柱箱温度55 ℃, 载气为高纯N2, 进样量1 mL, 流量35 cm3·min-1.
由于本实验采用的是静态培养的泥浆法探究底泥的反硝化速率, 并未考虑水动力等其他因素产生的影响, 因此, 本文基于此次实验对全湖反硝化量进行的估算存在一定的局限性.静态的泥浆法将沉积物和乙炔混匀有利于快速测定反硝化产物N2O的产生速率, 具有简单、便捷的优点.但因为在反硝化反应中硝酸盐被转化和被消耗, 忽略了水动力作用下, 水体硝酸盐向沉积物扩散和补充被消耗硝酸盐的作用, 从而导致测定的反硝化速率偏低.
2.3 反硝化速率计算沉积物反硝化作用的强度(F), 即单位时间内单位面积土壤产生的N2O量(μmol·m-2·h-1), 计算公式见式(1).
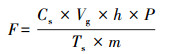 | (1) |
2.4 其他处理和分析使用剩余原状沉积物样品测算其基本理化指标.使用烘箱烘干沉积物样品, 计算其含水率;将烘干样品研磨, 过100目尼龙筛, 使用重铬酸钾油浴法测定有机碳(鲍士旦, 2000);用1 mol·L-1的KCl溶液提取新鲜沉积物中的铵氮, 振荡1 h后, 在3000 r·min-1转速下离心10 min后过滤上清液, 在4 ℃环境下保存, 利用分光光度法测定沉积物样品中铵氮含量(高凤鸣等, 1980).
3 结果(Results)3.1 采样点沉积物理化指标对所有样品测试其含水率、TOC、NH4+-N含量, 结果见表 1.其中, 春季样品含水率变异系数为0.25, 夏季样品含水率变异系数为0.26, 说明春季和夏季样品含水率波动差异不大;春季样品TOC含量变异系数为0.18, 夏季样品TOC含量变异系数为0.45, 夏季样品的有机碳含量波动远大于春季, 且变化范围更大;春季样品NH4+-N含量变异系数为0.52, 夏季样品NH4+-N含量变异系数为1.09, 两季NH4+-N含量波动都很大, 且夏季含量波动显著大于春季.综合所用理化指标可得, 春季样品中的含水率、TOC、NH4+-N含量波动明显小于夏季, 这可能与夏季温度较高, 加速湖底淤泥的多种生化反应有关.
表 1(Table 1)
| 表 1 采样点位置描述及沉积物理化性质 Table 1 Sampling sites and the physicochemical parameters of the sediments | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
表 1 采样点位置描述及沉积物理化性质 Table 1 Sampling sites and the physicochemical parameters of the sediments
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
3.2 沉积物反硝化速率及其时空差异淀山湖沉积物春、夏两季上、下层反硝化速率(以N计)如图 2所示, 上层平均反硝化速率为(17.91±11.80) μmol·m-2·h-1, 下层为(11.02±10.40) μmol·m-2·h-1, 上层土壤具有较大的反硝化速率, 脱氮能力占到了总体的62%, 且随着土壤深度的增大, 反硝化速率明显降低, 上、下层反硝化速率差异显著(p<0.05).不论是春季还是夏季, 表层反硝化速率都显著高于下层, 这与大多数研究相符(Garcia-Ruiz et al., 1998b;Livingstone et al., 2000).同时, 上、下层沉积物的反硝化速率均呈现出明显空间差异, 但下层差异明显小于上层.
图 2(Fig. 2)
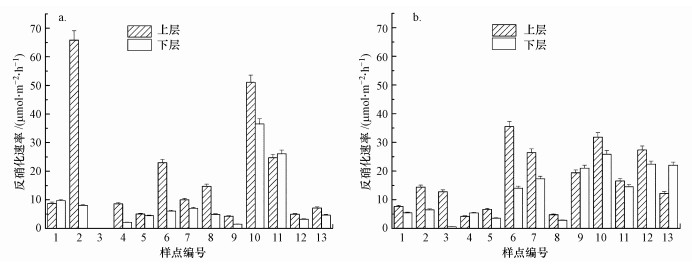 |
| 图 2 春(a)、夏(b)两季采样点上下层沉积物反硝化速率 Fig. 2The denitrification rate of upper and lower layers sediments in spring (a) and summer (b) |
春、夏两季反硝化速率为5.72~65.82 μmol·m-2·h-1, 存在明显的时空差异性.如图 3所示, 在13个采样点中, 12、1、2号采样点为出水口, 6、8、9、10号采样点为进水口, 其中以6、10号样点为主要进水口.春季, 上层沉积物的反硝化速率以出水口1、2号点最大, 进水口10号次之, 而下层沉积物则在10号进水口处反硝化作用最强.夏季, 各采样点间的反硝化速率差异并不大, 上、下层沉积物反硝化作用均以6、10号进水口与12号出水口最大.春季上层反硝化速率变异系数为1.04, 夏季上层反硝化速率变异系数为0.62, 说明夏季不同采样点之间的反硝化速率波动较小, 反硝化作用较春季对取样点空间变化不敏感.从季节变化来看, 春季上层平均反硝化速率为19.01 μmol·m-2·h-1, 夏季有所降低, 但仍维持在较高水平, 为16.90 μmol·m-2·h-1, 这种春季高于夏季的季节变化也在国内外的研究中出现过(Garcia-Ruiz et al., 1998a).综合上、下层沉积物, 得到6 cm沉积物的平均反硝化速率(图 4).
图 3(Fig. 3)
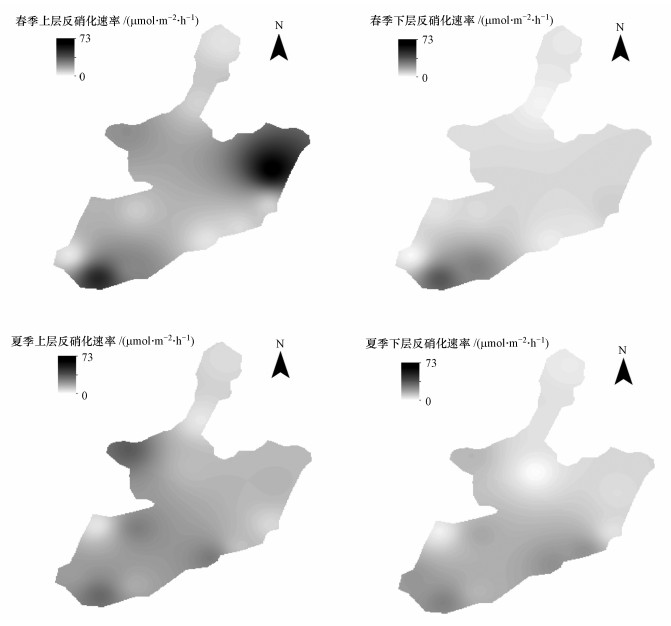 |
| 图 3 春、夏两季沉积物反硝化速率时空特征 Fig. 3The spatiotemporal characteristics of denitrification rates in two seasons |
图 4(Fig. 4)
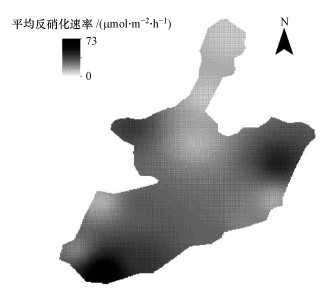 |
| 图 4 淀山湖6 cm沉积物平均反硝化速率插值图 Fig. 4Interpolation of the average denitrification rate of 6 cm sediment in Dianshan Lake |
4 讨论(Discussion)4.1 沉积物理化性质对反硝化速率的影响淀山湖沉积物中提取态的铵氮含量均值在春季较大(图 5), 但各个采样点的含量差异也较大, 受空间因素的影响较大, 在垂直方向上铵氮含量变化无明显规律;沉积物的含水率在春季明显较大, 且与空间位置有很大关系, 在夏季含水率显著减少, 数据波动程度也显著降低, 从垂直方向来看, 下层沉积物的含水量受空间影响更显著;淀山湖沉积物中有机碳含量在春季普遍较高, 且变异系数相对较小, 含量对空间位置变化不明显, 而夏季有机碳含量较春季低, 且波动较大.
图 5(Fig. 5)
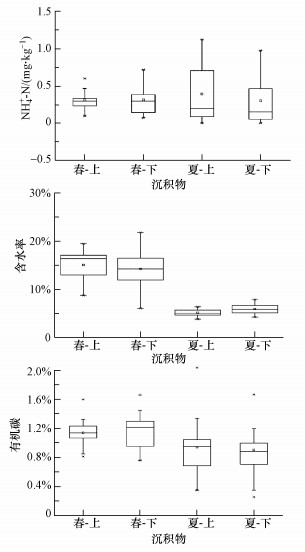 |
| 图 5 沉积物理化性质特征 Fig. 5Sedimentary physical and chemical factors |
4.2 沉积物铵氮含量与反硝化速率NH4+作为硝化反应的底物, 生成的NOx-在缺氧条件下进一步参与反硝化过程.根据硝化-反硝化耦合过程与同步硝化反硝化(SND)过程(Munch et al., 1996), 由于氧扩散的限制, 在沉积物表层产生溶解氧梯度和富氧区-厌氧区, 使得硝化与反硝化过程能够同步进行, 不断交换反应物与生成物, 形成一个完整的反馈系统, 因此, 铵氮的含量会对淀山湖湖底沉积物的反硝化速率产生影响.当铵氮含量较高时, 硝化反应加速生成NOx-, 为反硝化提供底物.由于反应物浓度上升, 反硝化速率提高, 沉积物铵氮含量与反硝化速率成正相关.相关分析结果表明, 反硝化速率与沉积物中NH4+-N含量呈显著正相关(p<0.05), 说明沉积物表层耦合的硝化-反硝化过程是沉积物反硝化的主要机制.同时, 反硝化速率在表层沉积物高于底层, 也验证了表层的耦合硝化-和反硝化过程占主导作用.
4.3 有机碳含量与反硝化速率有机碳通过影响反硝化微生物而影响反硝化进程, 但并不是土壤中所有的有机碳都能被反硝化微生物所利用, 有机碳的数量和质量对反硝化的进程有着不同程度的影响(Hill et al., 2004).Lalisse-Grundmann等(1988)利用乙炔抑制法研究有机碳对反硝化作用的影响, 结果表明, 增加碳源可使反硝化速率增加5倍以上.Garcia等(2003)发现, 在缺乏有机碳的土壤中, 添加简单有机碳(葡萄糖)会大幅度提高反硝化速率.理论上, 反硝化进程需要的C: N=1.25: 1(mol/mol)(吴耀国, 2002), 适当的有机碳在分解时能消耗土壤中的氧, 利于土壤中厌氧环境的形成, 从而促进反硝化进程(范晓晖等, 2002).碳氮比过低时, 缺氧条件不理想, 限制反硝化作用进程(Morris et al., 1988;Bradley et al., 1995); 碳氮比过大, 微生物活性降低, 反硝化作用亦会受到抑制(齐玉春等, 1999).而淀山湖底泥的反硝化速率与沉积物中有机碳含量相关性不显著(表 2), 说明在淀山湖底泥沉积物的反硝化作用中, 有机碳含量并非单一的显著影响因子.
表 2(Table 2)
| 表 2 淀山湖沉积物反硝化速率与理化性质相关关系 Table 2 Correlation analyses between the sedimentary denitrification rate and physical and chemical factors | ||||||||||||||||||||
表 2 淀山湖沉积物反硝化速率与理化性质相关关系 Table 2 Correlation analyses between the sedimentary denitrification rate and physical and chemical factors
| ||||||||||||||||||||
4.4 国内外反硝化速率的对比本研究中淀山湖沉积物平均反硝化速率为28.93 μmol·m-2·h-1.Risgaard-Petersen等(1998)研究了Sùbygaard Sù Lake的沉积物, 得出其反硝化速率为149.17 μmol·m-2·h-1, 显著高于本研究成果.利用N2生成法测定的北美休伦湖Saginaw湾1995年夏季沉积物反硝化速率为16.00~39.60 μmol·m-2·h-1 (Yang et al., 1998).本研究与徐徽等(2009)在太湖北部梅梁湾内湾测定结果(均值为36.37 μmol·m-2·h-1)及唐陈杰等(2014)在鄱阳湖洲滩沉积物中测定结果((35.36±6.12) μmol·m-2·h-1)类似.张波等(2012)利用15N同位素配对法对太湖流域江苏和上海境内主要河流沉积物的反硝化作用进行研究, 得出其夏季反硝化速率均值为32.92 μmol·m-2·h-1.
表 3(Table 3)
| 表 3 国内外不同湖区沉积物反硝化速率 Table 3 Denitrification rates of sediments in different lake areas at home and abroad | ||||||||||||||||||||||||||||
表 3 国内外不同湖区沉积物反硝化速率 Table 3 Denitrification rates of sediments in different lake areas at home and abroad
| ||||||||||||||||||||||||||||
4.5 水体沉积物脱氮能力通过淀山湖春、夏两季13个采样点的沉积物反硝化平均速率, 可得到整个湖区的插值数据, 由此估算淀山湖湖区上半年通过反硝化作用可去除约278.70 t的氮.研究表明, 随着土壤深度的增加, 反硝化作用减弱(邹国元等, 2001).土壤表层作为碳源和氮源输入的直接接触层, 是反硝化作用的活跃场所(Bernal et al., 2007)在本次研究中, 淀山湖上层0~3 cm土壤的脱氮能力占整个研究范围的62%, 即上层沉积物上半年可去除近172.80 t的氮.
5 结论(Conclusions)淀山湖沉积物6 cm原状土层的平均反硝化速率为28.93 μmol·m-2·h-1, 春季反硝化速率为(28.52±26.21) μmol·m-2·h-1, 夏季反硝化速率为(29.31±17.11) μmol·m-2·h-1.表层(0~3 cm)沉积物反硝化速率显著高于底层(3~6 cm)沉积物, 占总体反硝化速率的62%.沉积物NH4+-N含量与反硝化速率成显著正相关(p<0.05), 沉积物中耦合的硝化-反硝化过程是沉积物反硝化作用的主要机制.此外, 温度、有机碳含量对反硝化作用的影响更为复杂, 有待进一步的研究.研究估算整个湖区上半年通过反硝化作用可去除约278.70 t的氮.因此, 反硝化作用在淀山湖氮循环中具有重要意义, 是削减湖泊氮负荷、降低水体富营养化程度的有效途径.
参考文献
| 鲍士旦. 2000. 土壤农化分析[M]. 北京: 中国农业出版社. |
| Bernal S, Sabater F, Butturini A, et al. 2007. Factors limiting denitrification in a Mediterranean riparian forest[J]. Soil Biology and Biochemistry, 39(10): 2685–2688.DOI:10.1016/j.soilbio.2007.04.027 |
| Berelson W M, Heggie D, Longmore A, et al. 1998. Benthic Nutrient Recycling in Port Phi1lip Bay, Australia[J]. Estuarine, Coastal and Shelf Science, 46(6): 917–934.DOI:10.1006/ecss.1998.0328 |
| Bradley P M, McMahon P B, Chapelle F H. 1995. Effect of carbon and nitrate on denitrification in bottom sediments of an effluent-dominated river[J]. Water Resource Research, 31(4): 391–402. |
| 程曦, 李小平. 2008. 淀山湖氮磷营养物20年变化及其藻类增长响应[J]. 湖泊科学, 2008, 20(4): 409–419. |
| 范晓晖, 朱兆良. 2002. 旱地土壤中的硝化-反硝化作用[J]. 土壤通报, 2002, 33(5): 385–390. |
| Garcia-Montiel D C, Melillo J M, Steudler P A, et al. 2003. Carbon limitations to nitrous oxide emissions in a humid tropical forest of the Brazilian Amazon[J]. Biol, Fertile Soils, 38: 267–272.DOI:10.1007/s00374-003-0637-y |
| Garcia-Ruiz R, Paninson S N, Whitton B A. 1998a. Denitrification and nitrous production in sediments of the Wiske, a lowland eutrophic river[J]. Science of the Total Environment, 210(98): 307–320. |
| Garcia-Ruiz R, Pattinson S N, Whitton B A. 1998b. Denitrification in sediments of the freshwater tidal Yorkshire Ouse[J]. Science of the Total Environment, 210/211: 321–327.DOI:10.1016/S0048-9697(98)00021-7 |
| Groffman P M, Altabet M A, Bohlke J K, et al. 2006. Methods for measuring denitrification:Diverse approaches to a difficult problem[J]. Ecological Applications, 16(6): 2091–2122.DOI:10.1890/1051-0761(2006)016[2091:MFMDDA]2.0.CO;2 |
| 高凤鸣, 张淑华, 汪心源, 等. 1980. 用次溴酸钠氧化法测定海水中氨氮的研究[J]. 海洋湖沼通报, 1980(4): 41–46. |
| Hill A R, Cardaci M. 2004. Denitrification and organic carbon availability in riparian wetland soils and sub-surface sediments[J]. Soil Science Society of America Journal, 68(1): 320–325.DOI:10.2136/sssaj2004.0320 |
| 何岩, 沈叔云, 黄民生, 等, 2012. 城市黑臭河道底泥内源氮硝化-反硝化作用研究[J]. 生态环境学报, 21(6): 1166-1170 |
| 康丽娟. 2012. 淀山湖沉积物碳、氮、磷分布特征与评价[J]. 长江流域资源与环境, 2012, 21(S1): 105–110. |
| Lalisse-Grundmann G, Brunel B, Chalamet A. 1988. Denitrification in a cultivated soil:optimal glucose and nitrate concentrations[J]. Soil Biology and Biochemistry, 20(6): 839–844.DOI:10.1016/0038-0717(88)90090-9 |
| Lawrence R P, Smith E E, Carol M G. 1965. The exchange of phosphate between estuarine and sediments[J]. Limnology and Oceanography, 21(2): 167–172. |
| Livingstone M W, Smith R V, Larghlin R J. 2000. A spatial study of denitrification potential of sediments in Belfast and Strangford Loughs and its significance[J]. Science of the Total Environment, 251/252: 369–380.DOI:10.1016/S0048-9697(00)00417-4 |
| 卢嘉, 李小平, 陈小华. 2010. 12.淀山湖总氮和总磷的时空模拟分布[J]. 环境监测管理与技术, 2010, 22(6): 32–38. |
| Messer J, BIezonik P L. 1983. comparison of denitriocatjon rate estimation techniques in a large, shallow lake[J]. Water Research, 17(6): 63l–640. |
| Morris J T, Whiting G J, Chapelle F H. 1988. Potential denitrification rates in deep sediments from the southeastern Coastal Plain[J]. Environmental Science & Technology, 22: 832–835. |
| Munch E, Lant P, Keller J. 1996. Simultaneous nitrification and denitrification in bench scale sequencing batch reactors[J]. Water Research, 30: 277–284.DOI:10.1016/0043-1354(95)00174-3 |
| 齐玉春, 董云社. 1999. 土壤氧化亚氮产生、排放及其影响因素[J]. 地理学报, 1999, 54(6): 534–542. |
| Risgaard-Petersen N, Nielsen L P, Blackburn T H. 1998. Simultaneous measurement of benthic denitrification, with the isotope pairing technique and the N2 flux method in a continuous flow-through system[J]. Water Research, 32(11): 3371–3377.DOI:10.1016/S0043-1354(98)00121-3 |
| Risgaard Petersen N, Rysgaatd S, Nielsen L P, et al. 1994. Diurnal variation of denitrificafion and nitrification in sediments colonized by benthic microphysics[J]. The American Society of Limnology and Oceanography, 39(3): 573–579.DOI:10.4319/lo.1994.39.3.0573 |
| Seitzinger S, Scott Nixon, Michael E Q, et al. 1980. Denitrification and N2O production in near-shore marine sediments[J]. Geochemical et Cosmochimica Acta, 44(11): 1853–1860.DOI:10.1016/0016-7037(80)90234-3 |
| Seitzinger S P, Nielsen L P, Caffrey J, et al. 1993. Denitrification measuring in aquatic sediments:a comparison of three method[J]. Biogeochemistry, 23: 147–167.DOI:10.1007/BF00023750 |
| Sundby B, Gobeil C, Silberberg N. 1992. The phosphorus cycle in coastal marine sediments[J]. Limnology and Oceanography, 37(6): 1129–1145.DOI:10.4319/lo.1992.37.6.1129 |
| 孙志高, 刘景双, 于君宝. 2010. 三江平原典型草甸小叶章湿地土壤的反硝化作用[J]. 农业系统科学与综合研究, 2010, 26(1): 117–122. |
| 唐陈杰, 张路, 杜应旸, 等. 2014. 鄱阳湖湿地沉积物反硝化空间差异及其影响因素研究[J]. 环境科学学报, 2014, 34(1): 202–209. |
| 吴雅丽, 许海, 杨桂军, 等. 2014. 太湖水体氮素污染状况研究进展[J]. 湖泊科学, 2014, 26(1): 19–28.DOI:10.18307/2014.0103 |
| 吴耀国. 2002. 地下水中反硝化作用[J]. 环境污染治理技术与设备, 2002, 3(3): 27–31. |
| 徐徽, 张路, 商景阁, 等. 2009. 太湖梅梁湾水土界面反硝化和厌氧氨氧化[J]. 湖泊科学, 2009, 21(6): 775–781.DOI:10.18307/2009.0604 |
| 徐继荣, 王友绍, 孙松. 2004. 海岸带地区的固氮、氨化、硝化与反硝化特征[J]. 生态学报, 2004, 24(12): 2907–2914.DOI:10.3321/j.issn:1000-0933.2004.12.036 |
| 杨虹. 2010. 淀山湖浮游植物群落时空分布及与环境因子关系的研究[D]. 上海: 华东师范大学 |
| Yang L Y, Gardner W S. 1998. The sediment denitrification rates measurement and their spatial and temporal character analysis in Saginaw Bay, Lake Huron[J]. Journal of Lake Sciences, 10(3): 32–38.DOI:10.18307/1998.0306 |
| 张波, 杜应旸, 陈宇炜, 等. 2012. 太湖流域典型河流沉积物的反硝化作用[J]. 环境科学学报, 2012, 32(8): 1866–1873. |
| Zhong J C, Fan C X, Zhang L, et al. 2010. Significance of dredging on sediment denitrification in Meiliang Bay, China:A year long simulation study[J]. Journal of Environmental Sciences, 22(1): 68–75.DOI:10.1016/S1001-0742(09)60076-0 |
| 邹国元, 张福锁, 李新慧. 2001. 下层土壤反硝化作用的研究[J]. 植物营养与肥料学报, 2001, 7(4): 379–384.DOI:10.11674/zwyf.2001.0404 |
