 |
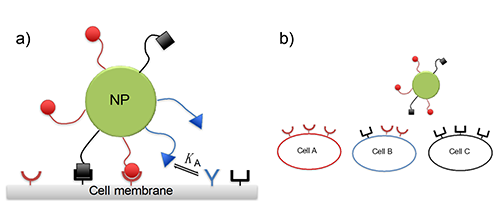
| 图1. 该研究模式图:(a)纳米粒子(NP)正在靶向到几种类型的受体上。 研究的主要的挑战是在纳米粒子上设计配体的组成以达到最高的选择性,比如(b)只靶向到B细胞,而不是A细胞或者是C细胞。 |
该理论的主要成果是设定简单的规则,利用多价颗粒和靶细胞的受体特性来区分进而靶向靶细胞:
1)主体(靶细胞)上受体的高敏特性是通过多价性来实现的,而不是通过客体(递送载体)上的配体和靶细胞上受体之间的强结合来实现的, 客体包覆更多的配体只会使其与主体上的受体产生微弱的结合。
2)在客体和主体表面的浓度分布应是密度匹配的。
3)配体-受体间相互作用的有效值约为1.3 kBT。
不同于传统的生物医学方法,这项工作中制定的规则是首先识别一个标记(高表达受体),然后找到一个能够有效并特定结合这个标记的配体(抗体)。抗体不具有选择性,他们能够强力依附在靶细胞上,同时也能够依附在其他具有类似膜成分的细胞上。因此,在癌症治疗中,药物会被同时传递到癌细胞和健康细胞(如肝细胞、肾细胞等等)上,严重制约了化疗的效率。这表明,药物的选择性传递只能通过具有弱结合作用的多价载体来实现。这项工作所得到的结果证明,副作用明显降低的定向性药物传递是可以实现的!
这项研究的标题为 “Optimal multivalent targeting of membranes with many distinct receptors”发表在美国国家科学院院刊上。 这项研究受到来自中国科学院物理研究所和欧洲与英国的资助。
论文链接http://www.pnas.org/content/early/2017/06/20/1704226114
注:该新闻原稿由Jure Dobnikar 教授和Tine Curk 博士提供,中文版由李涛博士翻译提供, 如有不清楚之处,请参考附件原稿。
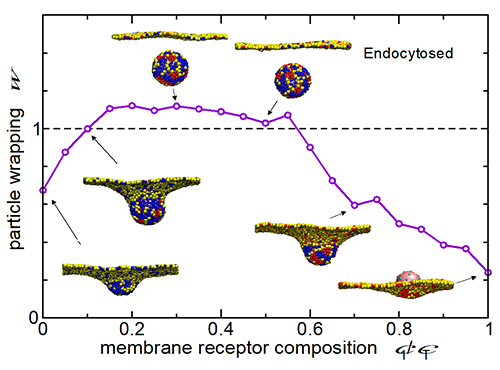 |
| 图2. 通过粒子表面构造设计控制纳米粒子由内吞进入细胞膜的速率 |
 |
| 图3. 客体吸附(符号)的巨正则系宗蒙特卡洛模拟与分析理论(实线)的比较。 相应模拟的快照展示于上方。 模拟的表面有两种不同类型的受体(分别为橘色和蓝绿色)。 |
Advances in Designing Cell Targeting Strategies-SM9-DOBNIKAR Jure.pdf
PNAS-2017-Curk-published_paper.pdf
