III型CRISPR-Cas系统的效应复合物(effector complex)可以分为III-A和III-B两个亚型,它们的特点是具有Cas10蛋白(III-A中被称为Csm1,III-B中为Cmr2),Cas10通过和其他多个Csm/Cmr亚基及一条crRNA(CRISPR RNA)组装成效应复合物。该效应复合物既可以降解RNA也可以降解DNA(ssDNA)。当外源基因入侵宿主后,该复合物通过“扫描”入侵者转录的RNA以找到与crRNA的guide区域互补的target RNA并与之结合,进而激活Csm3/Cmr4亚基降解此段RNA;同时,该复合物中Cas10的ssDNase活性也被激活,从而将与转录产物相关的ssDNA降解[3];2017年,该系统的另一种独特的调节机制被揭示,当target RNA出现时,III-A型CRISPR-Cas效应复合物具有腺苷酸环化酶的功能,环化的腺苷酸(cOAn)作为一种新型的第二信使来激活下游Csm6蛋白的非特异性RNA降解活性[4, 5]。
该系统如何通过特异性识别以防止误伤自身的RNA和DNA是人们关心的一个重要问题。生化研究表明,当target RNA序列与crRNA 5’-handle互补时,Cas10的ssDNase活性会被抑制,从而保护宿主DNA免于被降解;而当来自于外源基因的target RNA无法与crRNA 5’-handle互补配对时,则激活Cas10的ssDNase活性。然而,由于目前III-A型CRISPR-Cas效应复合物仅有几个低分辨率的电镜结构(17-30埃)[6, 7],所以对于III-A型CRISPR-Cas系统的若干问题,包括其效应复合物的组装形式,crRNA 5’-handle非互补target RNA激活Csm1的ssDNA切割活性的结构基础以及促使腺苷酸环化的结构机制是什么等并不清楚。
11月21日,中国科学院生物物理研究所江涛团队和王祥喜研究员等合作在Cell Research 杂志上发表了题为“Cryo-EM structure of Type III-A CRISPR effector complex”的研究论文。该论文解析了来源于T. onnurineus 的III-A型CRISPR-Cas效应复合物3.35埃的冷冻电镜结构(图A-B)。
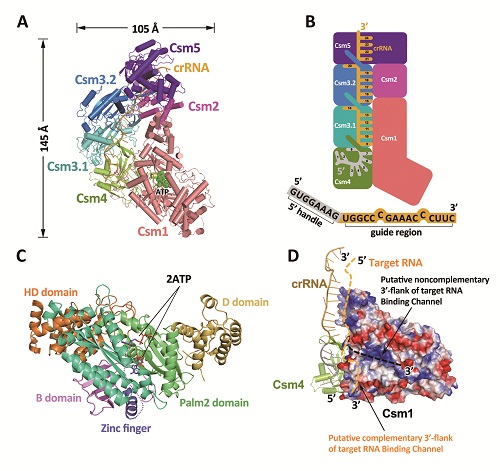
III-A型CRISPR-Cas效应复合物的结构生物学研究
A,T.onnurineus中III-A型CRISPR-Cas效应复合物的冷冻电镜结构全貌;B,A图中效应复合物所对应的模式图;C,ToCsm1和2个ATP分子的晶体结构图;D,ToCsm1的表面电势图及预测的target RNA结合通道,结合通道为图中虚线所示。
该项研究所报道的III-A型CRISPR-Cas效应复合物结构组成为Csm1121324151:crRNA,复合物整体呈“长靴”状,Csm1位于靴底,Csm1的C端和Csm2各形成一个‘helix bundle’并结合在一起组成靴筒,Csm4、Csm3.1、Csm3.2以及Csm5依次从靴底盘旋而上,和靴筒形成类似于双螺旋的结构。研究人员构建了一条5’端和Csm4结合,并自Csm4起始,贯穿Csm3.1、Csm3.2以及Csm5的crRNA,其中Csm4、Csm3.1及Csm3.2特定的β-sheet依次使得crRNA的8、14和20位碱基发生了翻转,表明了其降解位点,并得到了后续的生化实验验证。
此外,研究人员还解析了ToCsm1和2个ATP分子1.69埃分辨率的晶体结构,揭示了环化酶结合ATP分子的预反应状态(图C)。通过和其他相关结构的比较,发现ToCsm1的若干结构域的构象变化在宿主保护自我以及激活ToCsm复合物的ssDNA切割活性方面起重要作用(图D)。
该结构是目前第一个解析的原子分辨率水平的III-A型CRISPR-Cas效应复合物,为人们深入理解其功能提供了详实的结构基础。另一方面,过去的研究表明,III-A型CRISPR-Cas系统通过组装不同数目的Csm3和Csm2,以用于结合不同长度的crRNA。但在该报道的结构中,仅仅含有2个Csm3,和1个Csm2,因此这是目前报道的组成最为简单的III型CRISPR-Cas效应复合物。由于它的体量较小这一特点,也为将其改造成新的基因编辑工具提供了可能性和便利条件。
霍艳高博士、博士生李涛和博士生王男为该文章的共同第一作者。霍艳高博士、王祥喜研究员和江涛研究员共为本文的通讯作者。该项目得到了中国科学院先导项目以及国家自然科学基金的支持。
文章链接:https://www.nature.com/articles/s41422-018-0115-6
参考文献:
1. Makarova KS, Wolf YI, Alkhnbashi OS, Costa F, Shah SA, Saunders SJ, Barrangou R, Brouns SJ, Charpentier E, Haft DH et al: An updated evolutionary classification of CRISPR-Cas systems. Nature reviews Microbiology 2015, 13(11):722-736.
2. Tamulaitis G, Venclovas C, Siksnys V: Type III CRISPR-Cas Immunity: Major Differences Brushed Aside. Trends in microbiology 2017, 25(1):49-61.
3. Kazlauskiene M, Tamulaitis G, Kostiuk G, Venclovas C, Siksnys V: Spatiotemporal Control of Type III-A CRISPR-Cas Immunity: Coupling DNA Degradation with the Target RNA Recognition. Molecular cell 2016, 62(2):295-306.
4. Niewoehner O, Garcia-Doval C, Rostol JT, Berk C, Schwede F, Bigler L, Hall J, Marraffini LA, Jinek M: Type III CRISPR-Cas systems produce cyclic oligoadenylate second messengers. Nature 2017, 548(7669):543-548.
5. Kazlauskiene M, Kostiuk G, Venclovas ?, Tamulaitis G, Siksnys V: A cyclic oligonucleotide signaling pathway in type III CRISPR-Cas systems.pdf. Science 2017, 357:605–609.
6. Staals RH, Zhu Y, Taylor DW, Kornfeld JE, Sharma K, Barendregt A, Koehorst JJ, Vlot M, Neupane N, Varossieau K et al: RNA targeting by the type III-A CRISPR-Cas Csm complex of Thermus thermophilus. Molecular cell 2014, 56(4):518-530.
7. Rouillon C, Zhou M, Zhang J, Politis A, Beilsten-Edmands V, Cannone G, Graham S, Robinson CV, Spagnolo L, White MF: Structure of the CRISPR interference complex CSM reveals key similarities with cascade. Molecular cell 2013, 52(1):124-134.
(供稿:江涛课题组)
 附件下载:
附件下载: