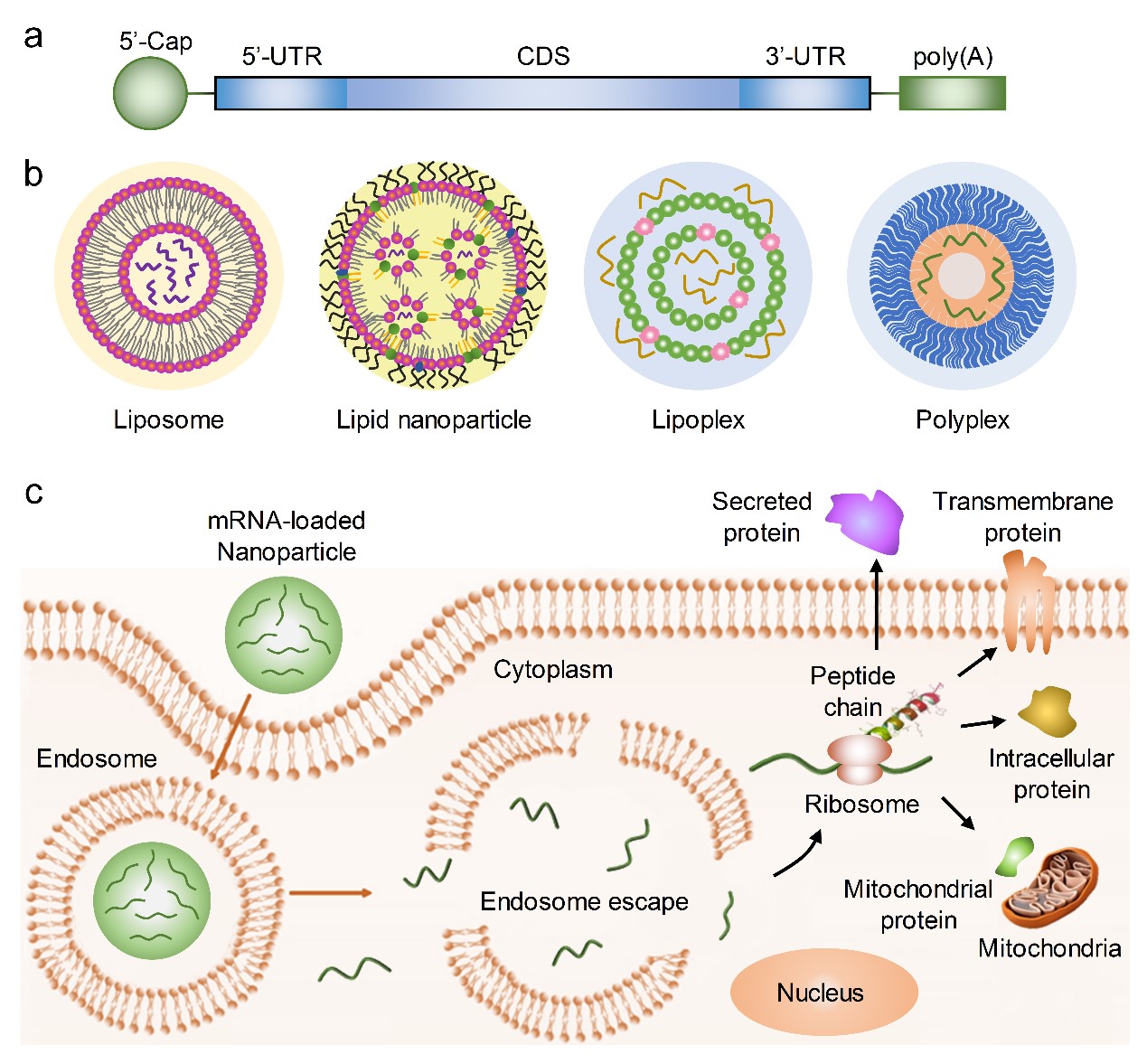
图1 mRNA疗法示意图。(a)体外转录mRNA的结构;(b)mRNA递送载体示意图;(c)mRNA入胞表达目的蛋白示意图
基于信使RNA(mRNA)、小干扰RNA(siRNA)、以及CRISPR/Cas(规律性间隔的短回文序列重复簇)等核酸物质的疾病防控技术,是未来生物医药领域最活跃、最重要的研究方向。其中,mRNA疗法可通过外源导入mRNA纠正基因表达缺陷或异常,或将表达抗原的mRNA制成疫苗。相较于传统的DNA基因治疗,mRNA疗法成本更低、表达蛋白更快,且没有基因整合风险。mRNA疗法业已成为近年来最具前景的前沿研究领域,mRNA疫苗和药物的相关研究正被快速推进,目前已有60余种mRNA制剂进入临床阶段。
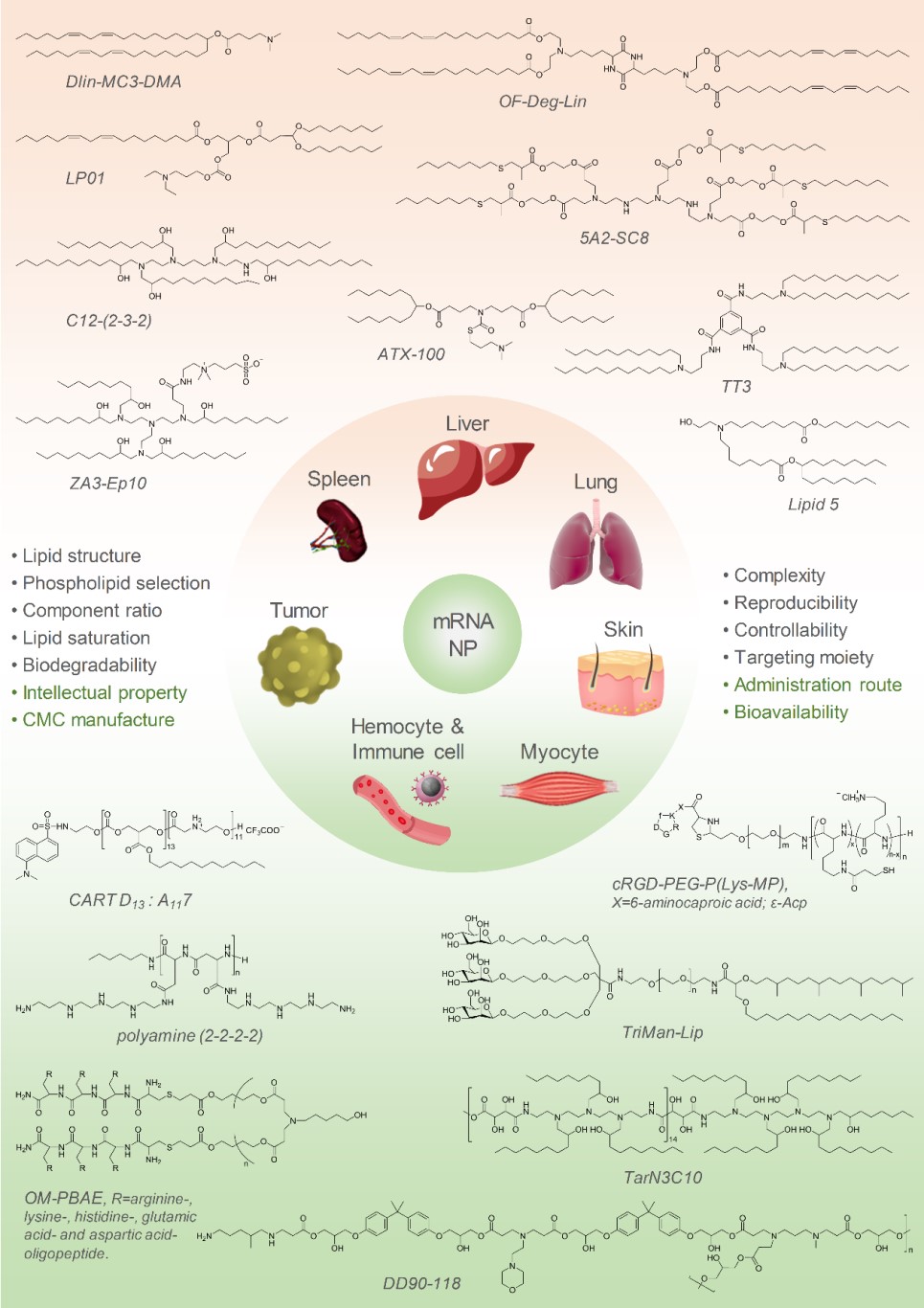
图2 代表性mRNA递送载体的结构与目标组织
该论文从mRNA的结构特征、制药关键技术、临床前与临床应用进展、挑战与机遇等几个方面详细论述了mRNA制药领域的现状与未来。重点讨论了mRNA制药领域的关键技术,包括结构修饰和递送技术,系统归纳了化学修饰的策略和递送材料的结构特征、组分配伍等(图2);阐述了mRNA在肿瘤疫苗、传染病疫苗、蛋白质替代治疗和细胞治疗领域的研究进展;也对目前已开展的mRNA临床试验和mRNA药物研发管线进行了梳理和总结。论文还指出,mRNA的稳定性和免疫原性已在很大程度上得到解决,但体内递送问题仍是最大的技术瓶颈,相较于分子量较小的siRNA和反义核酸(ASO),mRNA的递送难度更大、更具挑战性。该综述有望为从事mRNA疗法研究的科研工作者提供一份从原理到技术、从临床前探索到临床研究的完整线路图。
值得一提的是,黄渊余课题组基于前期在核酸技术方面的多年积累和专长,也正致力于mRNA疫苗和药物研究,包括mRNA递送技术的探索等。针对新近全球流行的新冠病毒肺炎,黄渊余团队主动担当,正积极与合作单位致力于mRNA疫苗的开发和新冠病毒核酸防治技术的攻关,目前已取得初步动物实验结果,研究工作也得到了光明日报的关注和报道。同时,黄渊余课题组关于siRNA制药的系统综述亦于2019年发表在Biotechnology Advances上(Biotechnology Advances, 2019, 37(5): 801-825)。黄渊余课题组相关研究成果得到了国家自然科学基金、中国博士后基金、北京理工大学科技创新计划创新人才资助专项等项目的资助。
附作者简介:
黄渊余,北京理工大学前沿交叉科学研究院研究员、课题组长、博士生导师,主要从事核酸技术与药物的相关研究,目前在Nano Lett、ACS Nano、Biotechnol Adv、Biomaterials等期刊发表SCI论文40余篇,论文总被引逾1800次,H-index为22;第一或通讯作者论文26篇,其中IF>10论文10篇,ESI高被引论文2篇(含热点论文1篇);参与撰写专著章节3部;申请专利3项。主持承担国家自然科学基金等项目近10项。是中国生物物理学会纳米生物学分会理事、秘书长,另4个学会理事或委员;是《Chinese Chemical Letters》等3个期刊编委;是Biomaterials等约30种SCI期刊的通讯审稿人;入选北京市科协青年托举人才(2019),获得中美纳米医学与纳米生物技术学会(CASNN)“Rising Star”奖(2019)等荣誉。
论文信息:
Weng Y, Li C, Yang T, et al. The challenge and prospect of mRNA therapeutics landscape. Biotechnol Adv. 2020;107534. doi:10.1016/j.biotechadv.2020.107534
https://www.sciencedirect.com/science/article/abs/pii/S0734975020300318
