该团队通过水热合成在镍钛合金表面构建出镍钛层状双氢氧化物(NiTi-LDHs)薄膜,该薄膜为碱性化合物,在肿瘤的微酸性环境下易降解,可释放毒性较大的镍离子,从而抑制癌细胞的生长;而在正常组织的弱碱性环境中,NiTi-LDHs薄膜稳定性较高,表现出良好的生物相容性(ACS Appl. Mater. Inter., 2015, 7(15) : 7843-7854.)。但上述薄膜对肿瘤抑制作用有限,还远达不到临床要求。为进一步提高其抗癌能力,该团队利用NiTi-LDHs表面丰富的羟基,通过聚苯乙烯磺酸钠修饰,实现了其对抗癌药物的负载,发现该载药系统表现出pH响应型药物释放行为,同时还可促进癌细胞对药物的吸收,能够有效杀伤癌细胞,但其对正常细胞也会造成较大损伤(ACS Appl. Mater. Inter.,2016, 8(37): 24491-24501)。为延缓药物释放速率,降低材料的系统毒性,该团队利用NiTi-LDHs的层状结构,将具有抗癌抗菌作用的丁酸根离子负载于NiTi-LDHs片层之间,发现上述载药平台具有微环境调节功能,可消耗肿瘤和炎症环境中的过氧化氢,同时释放丁酸根,显示较佳的抗癌抗菌作用,该工作以“Butyrate inserted Ni-Ti layered double hydroxide film for H2O2 mediated tumor and bacteria killing”为题发表于《今日材料》(Mater. Today, 2017, 20(5): 238-257)。
近日,该团队又在镍钛合金表面设计了一种金纳米棒修饰的NiTi-LDHs载药薄膜(Au@LDH/B)。由于金纳米棒具有较佳的光热效应,在近红外光辐照下,薄膜表面温度升高,NiTi-LDHs在高温作用下发生晶相转变,由层状双氢氧化物转变为层状双氧化物(LDOs),层间距减小,储存于NiTi-LDHs层间的药物随之释放,在热疗与化疗的协同作用下,肿瘤生长可被有效抑制。停止近红外光辐照后,薄膜晶型逆转变为层状双氢氧化物结构,环境中多余的药物分子“回流”至NiTi-LDHs层间,从而缓解药物对正常组织的损伤。该工作以“NIR-triggered crystal phase transformation of NiTi-layered double hydroxides films for localized chemothermal therapy”为题发表于Advanced Science(DOI: 10.1002/advs.201700782)。
上述系列研究工作得到国家自然科学基金委、中国科学院和上海市科委等项目的资助。
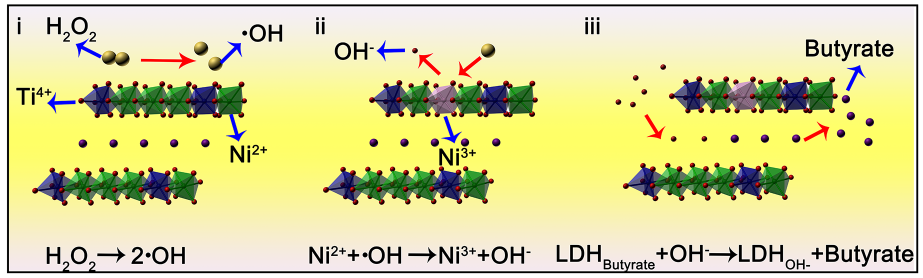
丁酸根负载NiTi-LDHs在过氧化氢作用下释放层间丁酸根
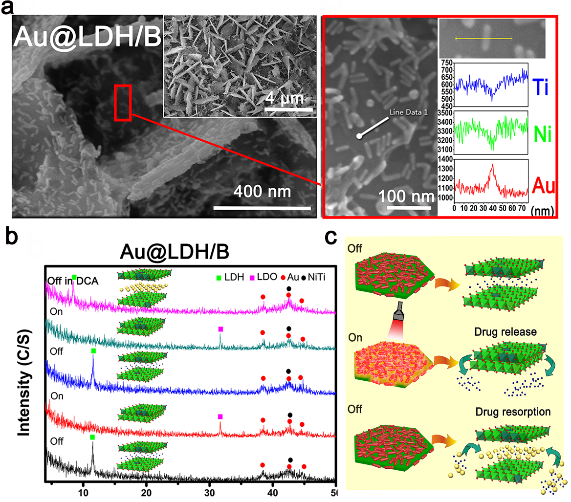
镍钛合金表面Au@LDH/B薄膜形貌(a),近红外光调节Au@LDH/B晶型转变(b),近红外光调节Au@LDH/B层间药物释放示意图(c)
