东北大学 冶金学院,辽宁 沈阳 110819
收稿日期:2022-02-28
基金项目:国家重点研发计划项目(2020YFC1806400,2018YFC1801200);中央高校基本科研业务费专项资金资助项目(N225037)。
作者简介:成丽(1998-),女,山西吕梁人,东北大学硕士研究生;胡恩柱(1985-),男,安徽淮南人,东北大学副教授,博士生导师。
摘要:针对有色金属采选场地存在重金属与残留选冶有机药剂复合污染问题,本文以丁基黄药(butyl xanthate, BX)为代表,基于饱和砂柱迁移实验和数学模型,分析了BX在石英砂、覆铁砂和覆铁铜砂中的迁移规律.结果表明,石英砂表面负载Fe量为0.07 mg/g时,BX迁移的回收率从89.8%下降至45.3%,并且负载Fe量每增加一倍,BX迁移回收率平均下降41.5%.在覆铁砂上继续负载氧化铜,BX与Cu2+之间反应生成CuBX,在负载Cu量0.010~0.055 mg/g时完全抑制了BX在介质中的迁移.
关键词:丁基黄药覆铁砂覆铁铜砂迁移数学模型
Transport Characteristics of Butyl Xanthate in Metal-Coated Quartz Sand
CHENG Li, LIANG Hai-jun, NAN Xiang-li, HU En-zhu


School of Metallurgy, Northeastern University, Shenyang 110819, China
Corresponding author: HU En-zhu, E-mail: huez@smm.neu.edu.cn.
Abstract: There is a combined pollution of heavy metals and residual organic agents for mineral dressing and smelting in nonferrous metal industry area. The transport behaviors of butyl xanthate (BX) in quartz sand, Fe-coated sand and Fe/Cu-coated sand were investigated using saturated sand column experiments and mathematic model. The results show that quartz sand loading Fe (0.07 mg/g) on the surface can reduce the recovery rate of BX from 89.8% to 45.3%, and it decreases by 41.5% with the doubling of iron content. When CuO was loaded subsequently on the Fe-coated sand, BX could react with Cu2+ to generate CuBX. And the transport of BX was completely inhibited when Cu was loaded within a range of 0.010~0.055 mg/g.
Key words: butyl xanthate (BX)Fe-coated sandFe/Cu-coated sandtransportmathematic model
有色金属采选过程中会使用大量的有机选矿药剂,诸如捕收剂(黄药、黑药、硫氨酯等)、起泡剂(松醇油、醚醇、甲酚等)和调整剂(羧甲基纤维素、丹宁等)[1].部分有机药剂残留在选矿废水或废渣中,最终随地表径流或地下渗滤进入水体和土壤,从而污染矿区及其周边生态环境[2].黄药(烃基二硫代碳酸盐,又称为烃基黄原酸盐)是有色金属硫化矿浮选过程中最常用、最重要的一类捕收剂.有研究表明,在选矿各环节产生的废水中,黄药质量浓度最高可达4~6 mg/L.通常黄药质量浓度大于0.1 mg/L即会对水生生物产生负面影响[3].黄药还会对土壤微生物活性和土壤酶活性产生较长时间的抑制作用[4].在环境介质中残留的黄药还可能与重金属发生络合作用,从而改变彼此的迁移转化行为,增加矿区的复合污染风险.目前研究的重点主要集中在黄药的降解机理方面,包括光催化降解[5-6]、高级氧化降解[7-9]和微生物降解[10-11].而关于黄药在土壤和地下水中迁移特性的研究相对较少,尤其是针对介质中存在的重金属矿物对黄药迁移过程的吸附和拦截机制尚属空白,极大地限制了对其环境风险的客观评价.
本文以丁基黄药(butyl xanthate,BX)为研究对象,基于饱和砂柱迁移实验和等温吸附实验,结合数学模型,分析BX在石英砂和金属负载石英砂中迁移的动力学特征,揭示不同金属对BX迁移的影响机理,以期为预测BX在土壤和地下水的环境行为提供基础.
1 材料和方法1.1 试剂和仪器主要试剂:石英砂、丁基黄药(BX)、NaCl、CuSO4·5H2O、Fe(NO3)3·9H2O、NaOH、HCl,均为分析纯,购自国药集团化学试剂有限公司.
主要仪器:数控自动部分收集器(SBS-100,上海沪西分析仪器厂有限公司)、蠕动泵(BT100-2J,河北保定兰格恒流泵有限公司)、紫外-可见分光光度计(752N,上海佑科仪器仪表有限公司)、往复振荡器(HY-2,金坛市富华仪器有限公司)、离心机(L420,湖南湘仪离心机有限公司)、冷冻干燥机(FD-1A-5,北京博医康实验仪器有限公司)、傅里叶变换红外光谱仪(Nicolet iS10,美国塞默飞世尔公司)、X射线衍射仪(SmartLab,日本理学株式会社)、X射线光电子能谱仪(Thermo Scientific K-Alpha+,美国赛默飞世尔公司)、场发射扫描电镜(ZEISS Gemini 300,卡尔蔡司上海管理有限公司)、原子吸收分光光度计(TAS-990,北京普析通用仪器有限责任公司).
1.2 材料制备石英砂平均粒径为0.6 mm,使用前用浓盐酸浸泡24 h,然后用去离子水反复清洗至上清液pH为中性,最后在105 ℃条件下烘干至恒重.
以处理后的石英砂为原料制备覆铁砂.烧杯中加入35 mL浓度为0.17 mol/L的Fe(NO3)3·9H2O溶液并置于磁力搅拌器上,然后逐滴加入36 mL浓度为0.52 mol/L的NaOH溶液.将混合液倒入装有200 g石英砂的聚四氟乙烯烧杯,搅拌均匀后,置于105 ℃烘箱中72 h.前6 h每隔1 h搅拌一次,以防止石英砂表面粘连.烘干后取出,常温冷却.将制备好的覆铁砂置于200 mL浓度为1 mol/L HCl溶液中静置10 min,洗去未附着物.之后用去离子水反复清洗至上清液电导率小于5 μS/cm,清洗完成后置于105 ℃烘箱中烘干至恒重[12].
以类似的方法制备负载在石英砂表面的铁矿物.具体操作步骤为:聚四氟乙烯烧杯中加入250 mL浓度为0.5 mol/L的Fe(NO3)3·9H2O溶液后置于磁力搅拌器上,之后逐滴加入200 mL浓度为2.5 mol/L的NaOH溶液,置于70 ℃烘箱中120 h.将得到的固体用去离子水以离心方式反复清洗至上清液pH为中性.清洗完成后冷冻干燥24 h,之后研磨过0.074 mm筛,保存于广口瓶中备用.
以制得的覆铁砂为原料制备覆铁铜砂.烧杯中加入12 mL浓度为0.06 mol/L的CuSO4·5H2O溶液后置于磁力搅拌器上,之后逐滴加入4 mL浓度为0.52 mol/L的NaOH溶液[13].将混合液加入制备的覆铁砂中,搅拌均匀.后续烘干、清洗等步骤同覆铁砂的制备过程.制备好的石英砂、覆铁砂和覆铁铜砂均保存于聚乙烯瓶中备用.
铁铜复合矿物的制备过程如下:烧杯中加入250 mL浓度为0.5 mol/L的Fe(NO3)3·9H2O溶液后置于磁力搅拌器上,逐滴加入200 mL浓度为2.5 mol/L的NaOH溶液.于另一个烧杯中加入52.8 mL浓度为0.29 mol/L的CuSO4·5H2O,再次逐滴加入17.6 mL浓度为2.5 mol/L的NaOH溶液.两批溶液导入聚四氟乙烯烧杯混合,置于70 ℃烘箱中120 h.后续清洗、冻干、研磨等步骤同铁矿物的制备.
1.3 等温吸附实验取2 g石英砂或金属负载砂加入30 mL不同质量浓度(0,0.5,1,2,4,8 mg/L)的BX溶液中,于25 ℃避光振荡4 h,然后静置15 min.取上清液于301 nm波长下测定吸光度,根据标准曲线换算BX浓度.平衡吸附量计算如式(1)所示:
 | (1) |
为推测吸附机理,以铁矿物和铁铜复合矿物作为吸附剂,分析它们吸附BX前后的红外光谱特征.具体操作如下:分别称取0.3 g矿物于顶空瓶中,加入30 mL浓度为0.01 mol/L的BX溶液,于25 ℃恒温振荡4 h.吸附平衡后,将全部物质过0.22 μm滤膜,之后将滤膜冷冻干燥,取固体粉末进行傅里叶变换红外光谱检测.
1.4 砂柱迁移实验迁移实验在高度10 cm、内径为2.74 cm的玻璃柱内进行.采用干法分段装填介质,每装填1 cm轻敲玻璃柱外壁使介质均匀紧实分布.在玻璃柱两端分别放置0.15 mm的不锈钢筛网防止石英砂流出.实验以洁净石英砂为对照,将制得的金属负载石英砂与洁净石英砂按一定比例混合获得不同含铁量的覆铁砂或覆铁铜砂,具体实验设计如表 1所示.每个柱子装填石英砂或金属负载石英砂质量约(84.0±2.0)g.
表 1(Table 1)
| 表 1 丁基黄药砂柱迁移实验处理 Table 1 Treatments of sand column experiments for BX transport |
利用蠕动泵自下而上以0.3 mL/min流量通入溶液,柱子上端流出的溶液通过自动收集器定时收集.实验前,通入12 h的背景溶液(去离子水)饱和砂柱.从零时刻起,通入4 mg/L的BX溶液320 min;紧接着通入背景溶液(去离子水)反冲200 min.每隔10 min收集流出液测定BX浓度.实验中全程避光以防止BX光解.
1.5 指标测定方法BX的浓度采用紫外分光光度法(301 nm)测定;介质和矿物的铁、铜元素含量采用火焰原子吸收分光光度法测定;采用能谱扫描电镜观察材料表观形貌;采用X射线衍射仪分析矿物组成;采用傅里叶变换红外光谱仪分析介质表面吸附黄药后的官能团特征;采用X射线光电子能谱仪分析介质表面的元素价态.
2 数学模型用两种不同的数学模型比较BX在砂柱中的迁移过程.一种是描述溶解态污染物迁移的一维对流弥散方程结合双点位化学非平衡吸附(two-site chemical nonequilibrium sorption,TSCNS)模型[14].
 | (2) |
 | (3) |
假设BX在石英砂和金属负载石英砂表面的吸附服从Freundlich-Langmuir特征,
 | (4) |
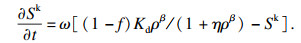 | (5) |
另一种模型是描述胶体态金属黄药络合物迁移的一维对流弥散方程结合双动力学点位附着-分离(two kinetic sites attachment-detachment,TKSAD)模型[15].
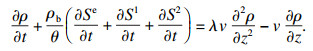 | (6) |
 | (7) |
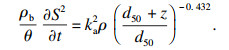 | (8) |
采用Hydrus-1D软件(版本4.16.0110,PC-Progress公司,捷克)对穿透曲线进行拟合.以Br-为示踪剂,根据其穿透曲线反演求解λ;Kd, η和β通过拟合等温吸附方程获取.基于赤池信息准则(Akechi information criterion,AIC)优选模型形式并推测迁移机理.
3 结果与讨论3.1 介质属性本文所制备的覆铁砂、覆铁铜砂及其表面所覆矿物的微观形貌如图 1所示.这些针状或棒状的铁、铜矿物堆积在石英砂表面的孔穴之中.由于石英砂表面整体较为光滑,比表面积较小,因此金属负载率较低(覆铁砂中铁质量分数为2.8%;覆铁铜砂铁质量分数为4.0%,铜质量分数为0.6%).对铁矿物和铁铜复合矿物进行XRD分析(图 2),结果表明二者分别为针铁矿(铁质量分数为49.1%)以及针铁矿和氧化铜的复合物(铁质量分数为47.3%,铜质量分数为7.5%).
图 1(Fig. 1)
 | 图 1 不同样品的SEM图(右上角小图为实物照片)Fig.1 SEM images of different samples(the small picture on the upper-right corner is the physical photo) (a)—石英砂;(b)—覆铁砂;(c)—覆铁铜砂;(d)—铁矿物;(e)—铁铜复合矿物. |
图 2(Fig. 2)
 | 图 2 金属矿物的XRD检测结果Fig.2 XRD results of metal minerals |
3.2 吸附机理由图 3可看出,石英砂对BX的吸附能力较弱,覆铁砂的吸附能力略强,二者在一定范围内都为接近线性的Freundlich形式.而覆铁铜砂对BX的吸附量较大,且更趋向于Langmuir形式.线性模型可用于描述吸附质初始质量浓度较低时的单层吸附过程,Freundlich模型主要用于描述非均质表面的多层物理吸附过程,而Langmuir模型则主要用于描述均质表面的单层化学吸附以及内扩散[16].
图 3(Fig. 3)
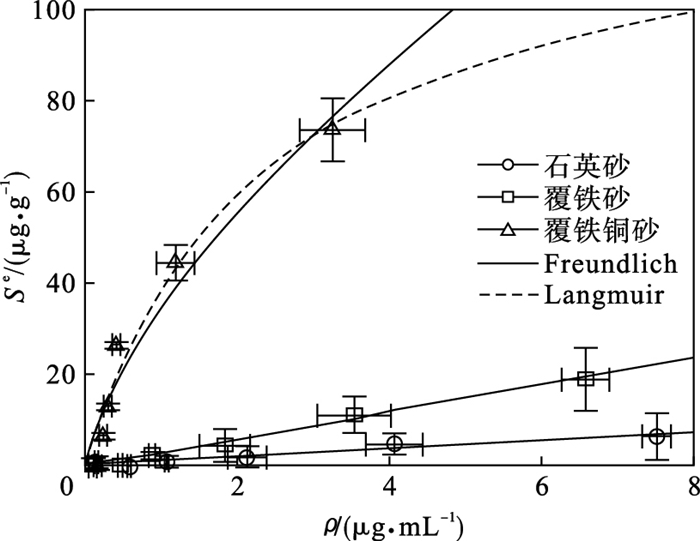 | 图 3 石英砂、覆铁砂、覆铁铜砂对丁基黄药的等温吸附特征Fig.3 Adsorption isotherms of BX by quartz sand, Fe-coated sand and Fe/Cu-coated sand |
Kd可用来评价BX在介质表面吸附亲和力的大小.模型拟合结果(表 2)显示覆铁砂吸附BX的Kd值大约是石英砂体系的2.4倍,表明负载针铁矿在一定程度上提高了介质对BX的吸附能力;而覆铁铜砂体系的Kd值约是覆铁砂的20.3倍,说明微量氧化铜的存在大大增强了介质对BX的吸附.
表 2(Table 2)
| 表 2 等温吸附模型参数拟合结果 Table 2 Parameter fitting results of isothermal adsorption model |
图 4a为铁矿物(即针铁矿)吸附BX前后的红外光谱图.其中,637 cm-1处为Fe—O/Fe—OH键的振动峰;794 cm-1和890 cm-1处为δ(OH)/γ(OH) 的变形振动;1 383 cm-1处为NO3-的特征峰(由于制备过程中使用了硝酸铁);1 638 cm-1处为水分子的弯曲振动[17].通过对比吸附前后的谱图可以看出,针铁矿吸附BX后没有出现明显的新特征峰,推测其对BX的吸附以物理吸附为主.
图 4(Fig. 4)
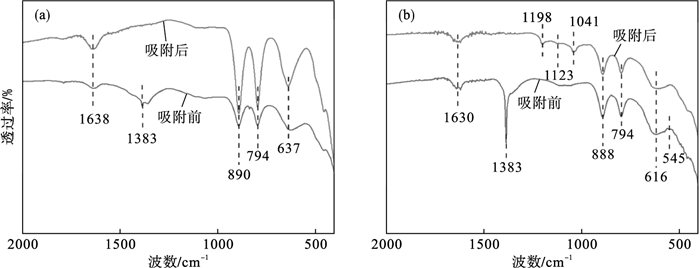 | 图 4 不同矿物吸附丁基黄药前后的红外光谱图Fig.4 FTIR spectra of different minerals before and after BX adsorption (a)—针铁矿; (b)—针铁矿复合氧化铜. |
图 4b为针铁矿复合氧化铜吸附BX前后的红外光谱图,545 cm-1处为Cu—O振动产生的特征峰;其余各谱峰的位置与图 4a类似.但是,铁铜复合矿物吸附BX后于1 041,1 123,1 198 cm-1处出现了新的特征峰.它们分别对应C═S键的伸缩振动、C—O—C对称伸缩振动以及C—O—C非对称伸缩振动.这说明CuO的负载使得介质表面对BX的吸附逐渐转变为化学过程.
为了进一步确定产物组成,对吸附BX前后的铁铜复合矿物进行XPS分析.图 5a显示吸附BX后样品的XPS全谱图中出现了S元素.对该样品S 2p进行分峰拟合,由图 5b可知,特征峰S 2p3/2和S 2p1/2结合能分别位于162.2 eV和163.5 eV,该峰可能归属于黄药本身或铜黄药中的S原子[18].图 5c结果表明,吸附BX前样品Cu 2p3/2特征峰的结合能位于933.18 eV,Cu 2p3/2峰形较宽,高结合能端有明显的振激峰,表明此时的Cu主要以Cu2+形式存在.然而在吸附BX之后,样品Cu 2p3/2特征峰的结合能略有下降(932.14 eV),Cu 2p3/2峰形变得尖锐,半峰宽减小,并且振激峰消失.另外,吸附BX后Cu俄歇谱峰的动能由917.8 eV降至916.8 eV,如图 5d所示.这说明吸附BX以后,样品中Cu组分所处的化学环境和能量状态发生了改变,原来的Cu2+全部被还原为低价态的Cu+.因此推定BX在铁铜复合矿物上的吸附产物为丁基黄原酸亚铜(CuBX),这与前人基于ATR-FTIR的研究结果相一致[19].
图 5(Fig. 5)
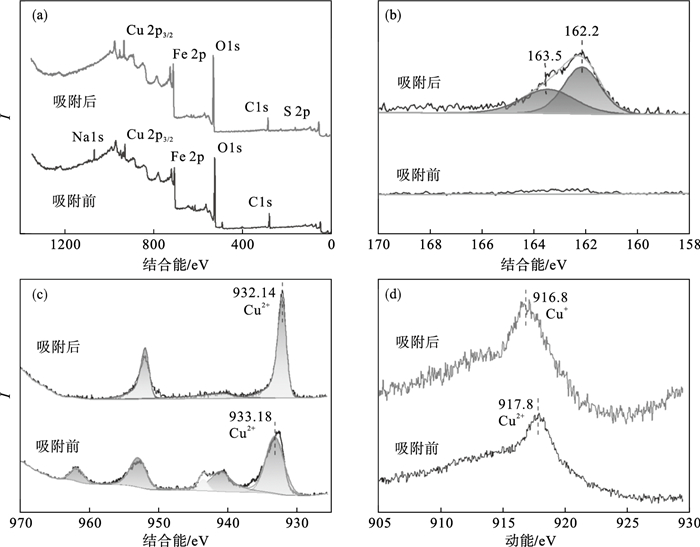 | 图 5 针铁矿复合氧化铜吸附丁基黄药前后的XPS分析谱图Fig.5 XPS analysis spectrums of goethite-CuO composite before and after BX adsorption (a)—XPS全谱;(b)—S 2p谱;(c)—Cu 2p谱;(d)—Cu俄歇谱. |
3.3 BX在不同介质中的迁移动态如图 6所示,BX在不同介质中的迁移存在显著的差异,其在石英砂中迁移的回收率可达89.8%,但是随着介质中铁、铜矿物的相继引入,BX的迁移能力显著下降(100%覆铁砂体系的回收率为15.5%), 甚至完全受到抑制(100%覆铁铜砂体系的回收率为零).由此推测石英砂表面负载的铁、铜矿物会通过物理、化学等吸附作用拦截BX,从而限制或阻止其在介质孔隙中的迁移.
图 6(Fig. 6)
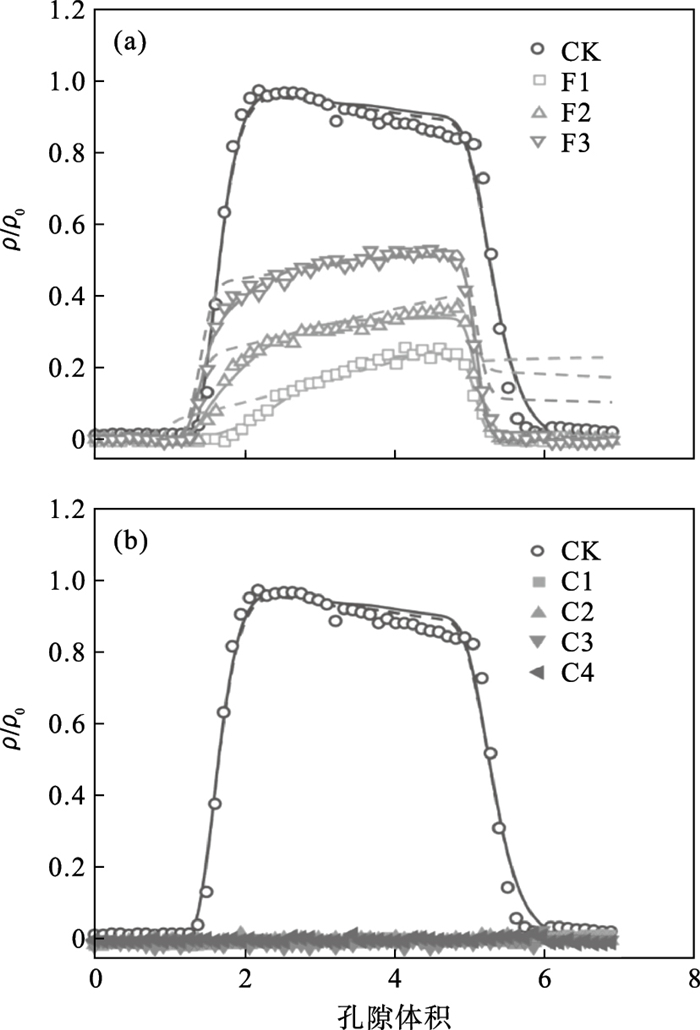 | 图 6 丁基黄药在石英砂、覆铁砂、覆铁铜砂中的穿透曲线Fig.6 Breakthrough curves of butyl xanthate in quartz sand, Fe-coated sand and Fe/Cu-coated sand (a)—覆铁砂与石英砂比较;(b)—覆铁铜砂与石英砂比较. |
由图 6a可以看出,随着介质中含铁量的增加,BX迁移能力逐渐降低.对于25%覆铁砂体系来说,BX迁移的回收率约为45.3%,当含铁量翻倍(50%覆铁砂),BX迁移的回收率降至28.2%.对TSCNS和TKSAD模型的拟合结果进行比较(表 3),结果表明BX在石英砂中的迁移更服从溶解态污染物(BX-)的迁移模式——TSCNS模型的AIC值较小.BX在石英砂表面的平衡吸附点位约占0.175,吸附过程以动力学-化学非平衡吸附为主,且吸附速率较慢,一级吸附速率系数ω仅为3.98×10-5 min-1.
表 3(Table 3)
| 表 3 BX穿透曲线的模型拟合结果 Table 3 Model fitting results of BX breakthrough curves |
BX在覆铁砂中的迁移行为明显倾向于胶体物质的迁移动态——TKSAD模型拟合结果的AIC值远小于TSCNS模型(表 3).由此推测,当介质表面存在针铁矿时,BX与介质表面的Fe3+发生反应生成六配位体丁基黄原酸铁Fe(BX)3,在浓度较低时以胶体形式存在,从而易被孔隙拦截而滞留在介质中.此外,Fe3+可将黄原酸根氧化为二黄原酸,即双黄药[(BX)2],后者可通过BX自由基以疏水作用的形式吸附在Fe(BX)3表面,从而加剧了BX的滞留[20].结合图 3的等温吸附结果可推测,BX与介质表面Fe3+发生吸附反应可能为单层吸附的线性形式,而双黄药在Fe(BX)3表面的吸附则使得吸附过程向多层物理吸附的Freundlich模型倾斜.BX在覆铁砂中迁移的模型拟合结果也证实,随着介质表面针铁矿含量的减少(实验处理F1至F3),TKSAD模型平衡点位所占的比例f并无显著差异,但是动力学点位的附着系数(ka1和ka2)逐渐降低,且第1动力学点位的最大附着量(Smax)逐渐下降(表 3),从而解释了介质对BX迁移的吸附拦截能力随着介质表面针铁矿含量的降低而逐渐减弱.
图 6b显示无论介质中含铜量高低(0.010~0.055 mg/g),BX的迁移都完全被抑制,并且这种抑制效应与介质表面的含铁量无关.这说明BX与Cu2+之间的反应较Fe3+要迅速得多,等温吸附实验的结果也表明该过程为单层化学吸附及内扩散(Langmuir形式).XPS分析结果表明其反应产物主要为丁基黄原酸亚铜(CuBX,图 5).但是也有文献报道这个过程仍伴有少量的双黄药产生,这些双黄药同样可以在疏水作用力的驱动下,以物理吸附的形式附着于CuBX的表面[20].但是很显然,CuBX的化学稳定性和沉降性能较Fe(BX)3要强很多,因而BX在覆铁铜砂中的迁移能力完全丧失.
4 结论1) BX在洁净石英砂介质中的迁移能力较强;当介质表面负载针铁矿以后,BX迁移的形式从溶解态转变为胶体态,BX与介质表面的Fe3+发生反应生成Fe(BX)3和双黄药,双黄药再以多层物理吸附的形式附着于Fe(BX)3表面,从而抑制了BX的迁移;并且负载铁量越高,BX迁移的回收率越低.
2) 当在覆铁砂表面继续负载氧化铜时,BX与Cu2+之间反应生成化学稳定性更好的CuBX,在负载铜量0.010~0.055 mg/g时完全抑制了BX在介质中的迁移,并且这种抑制作用与负载铁量无关.
参考文献
| [1] | 栾和林, 喻晗, 邹畅, 等. 复合污染状态下尾矿区有害化学品的迁移研究[J]. 环境化学, 2006, 25(2): 207-210. (Luan He-lin, Yu Han, Zou Chang, et al. Study on the migration rule of compound mineral processing reagents in tailing area of compound contamination[J]. Environmental Chemistry, 2006, 25(2): 207-210. DOI:10.3321/j.issn:0254-6108.2006.02.021) |
| [2] | Panayotova M. Impact of sulphide non-ferrous ore mining and dressing activities on the environment[J]. Journal of Environmental Science and Health Part A: Environmental Science and Engineering and Toxicology, 1997, 32(8): 2213-2228. DOI:10.1080/10934529709376678 |
| [3] | 孙乾予, 印万忠, 朱张磊, 等. 丁基钠黄药浮选斑铜矿的吸附热力学和动力学研究[J]. 东北大学学报(自然科学版), 2019, 40(4): 574-579. (Sun Qian-yu, Yin Wan-zhong, Zhu Zhang-lei, et al. Adsorption thermodynamics and kinetics of bornite using sodium butyl xanthate as collector in flotation[J]. Journal of Northeastern University(Natural Science), 2019, 40(4): 574-579.) |
| [4] | Li H, Yao J, Duran R, et al. Effects of typical flotation reagent on microbial toxicity and nickel bioavailability in soil[J]. Chemosphere, 2020, 240: 124913. DOI:10.1016/j.chemosphere.2019.124913 |
| [5] | Xiao Q, Ouyang L L. Photocatalytic photodegradation of xanthate over C, N, S-tridoped TiO2 nanotubes under visible light irradiation[J]. Journal of Physics and Chemistry of Solids, 2011, 72(1): 39-44. DOI:10.1016/j.jpcs.2010.10.087 |
| [6] | Zhang M, Han N, Fei Y, et al. TiO2/g-C3N4 photocatalyst for the purification of potassium butyl xanthate in mineral processing wastewater[J]. Journal of Environmental Management, 2021, 297: 113311. DOI:10.1016/j.jenvman.2021.113311 |
| [7] | Molina G C, Cayo C H, Rodrigues M A S, et al. Sodium isopropyl xanthate degradation by advanced oxidation processes[J]. Minerals Engineering, 2013, 45: 88-93. DOI:10.1016/j.mineng.2012.12.001 |
| [8] | García-Leiva B, Teixeira L A C, Torem M L. Degradation of xanthate in waters by hydrogen peroxide, fenton and simulated solar photo-fenton processes[J]. Journal of Materials Research and Technology, 2019, 8(6): 5698-5706. DOI:10.1016/j.jmrt.2019.09.037 |
| [9] | Lou J, Lu G, Wei Y, et al. Enhanced degradation of residual potassium ethyl xanthate in mineral separation wastewater by dielectric barrier discharge plasma and peroxymonosulfate[J]. Separation and Purification Technology, 2022, 282: 119955. DOI:10.1016/j.seppur.2021.119955 |
| [10] | Natarajan K A, Prakasan M R S. Biodegradation of sodium isopropyl xanthate by Paenibacillus polymyxa and Pseudomonas putida[J]. Minerals & Metallurgical Processing, 2013, 30(4): 226-232. |
| [11] | Chen S, Li S, Xiong P, et al. Biodegradation of sodium butyl xanthate by Shewanella oneidensis MR-1 in the presence of Cr(Ⅵ)[J]. Environmental Engineering Science, 2019, 36(9): 1179-1184. DOI:10.1089/ees.2018.0570 |
| [12] | Qi Z, Du T, Ma P, et al. Transport of graphene oxide in saturated quartz sand containing iron oxides[J]. Science of the Total Environment, 2019, 657: 1450-1459. DOI:10.1016/j.scitotenv.2018.12.143 |
| [13] | 杨翾. 铁铜氧化物复合改性石英砂滤料制备工艺与吸附特性研究[D]. 广州: 广东工业大学, 2016. (Yang Xuan. Study on the preparation process and adsorption characteristic of Fe/Cu oxide composite modified quartz sand[D]. Guangzhou: Guangdong University of Technology, 2016. ) |
| [14] | Hu E, Yuan H, Du Y, et al. LDPE and HDPE microplastics differently affect the transport of tetracycline in saturated porous media[J]. Materials, 2021, 14(7): 14071757. |
| [15] | Hu E, Shang S, Fu Z, et al. Cotransport of naphthalene with polystyrene nanoplastics(PSNP) in saturated porous media: effects of PSNP/naphthalene ratio and ionic strength[J]. Chemosphere, 2020, 245: 125602. DOI:10.1016/j.chemosphere.2019.125602 |
| [16] | Wang J, Guo X. Adsorption isotherm models: classification, physical meaning, application and solving method[J]. Chemosphere, 2020, 258: 127279. DOI:10.1016/j.chemosphere.2020.127279 |
| [17] | 杜玲. 铁氰离子在针铁矿表面吸附行为及吸附机制探究[D]. 重庆: 重庆大学, 2019. (Du Ling. Adsorption behavior of ferricyanide on goethite surface and exploration of adsorption mechanism[D]. Chongqing: Chongqing University, 2019. ) |
| [18] | Mikhlin Y L, Karacharov A A, Likhatski M N. Effect of adsorption of butyl xanthate on galena, PbS, and HOPG surfaces as studied by atomic force microscopy and spectroscopy and XPS[J]. International Journal of Mineral Processing, 2015, 144: 81-89. DOI:10.1016/j.minpro.2015.10.004 |
| [19] | 沈琪, 范迎菊, 尹龙, 等. 丁基黄药在CuO表面吸附的二维连续在线原位ATR-FTIR光谱研究[J]. 物理化学学报, 2014, 30(2): 359-364. (Shen Qi, Fan Ying-ju, Yin Long, et al. Two-dimensional continuous online in situ ATR-FTIR spectroscopic investigation of adsorption of butyl xanthate on CuO Surfaces[J]. Acta Physico-Chimica Sinica, 2014, 30(2): 359-364.) |
| [20] | Zhang Y, Cao Z, Cao Y, et al. FTIR studies of xanthate adsorption on chalcopyrite, pentlandite and pyrite surfaces[J]. Journal of Molecular Structure, 2013, 1048: 434-440. DOI:10.1016/j.molstruc.2013.06.015 |