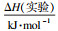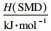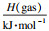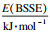, 张文馨, 李英华, 刘文刚
, 张文馨, 李英华, 刘文刚 东北大学 资源与土木工程学院, 辽宁 沈阳 110819
收稿日期:2021-11-12
基金项目:国家重点研发计划项目(2019YFC18038004); 沈阳市科技计划项目(22-322-3-01)。
作者简介:李海波(1974-), 男, 河北承德人, 东北大学教授, 博士生导师;
李英华(1979-), 女, 辽宁灯塔人, 东北大学教授, 博士生导师;
刘文刚(1981-), 男, 山东潍坊人, 东北大学教授, 博士生导师。
摘要:芳香族化合物在生物炭表面的分子行为、特别是弱相互作用机制尚不清楚.为揭示生物炭-苯酚间弱相互作用机制,本文采用等温吸附、吸附动力学实验,结合FT-IR表征,应用密度泛函理论(DFT),分析生物炭与苯酚分子间不同吸附构型的结合能、约化密度梯度(RDG)和电子密度拓扑关系.结果表明: 等温吸附经72 h达平衡,pH显著影响饱和吸附量,pH=6时吸附量最大; 生物炭表面官能团是吸附作用中心,吸附焓(ΔH)始终处于氢键键能范围内; 4种吸附构型(A/B/C/D)的弱相互作用均由范德华力和弱氢键共同主导,B构型结合能最低、最稳定,C构型弱相互作用最强,D构型弱相互作用最弱.
关键词:生物炭苯酚密度泛函理论氢键范德华力
Study on Mechanism of Weak Interaction Between Biochar and Phenol Based on Quantum Chemical Calculation
LI Hai-bo

 , ZHANG Wen-xin, LI Ying-hua, LIU Wen-gang
, ZHANG Wen-xin, LI Ying-hua, LIU Wen-gang School of Resources & Civil Engineering, Northeastern University, Shenyang 110819, China
Corresponding author: LI Hai-bo, E-mail: lihaibo@mail.neu.edu.cn.
Abstract: The molecular behavior of aromatic compounds on the biochar surface, especially the mechanism of weak interaction, is not yet clear. In order to reveal the mechanism of weak interaction between biochar and phenol, adsorption isotherm and adsorption kinetics experiments, as well as FT-IR characterization were used to analyze the binding energy, reduced density gradient (RDG) and electron density topological relationship between biochar and phenol of different adsorption configurations with density functional theory (DFT). Results showed that the adsorption isotherm reaches the equilibrium after 72h, pH significantly affects the saturated adsorption capacity, and the adsorption capacity is the largest at pH=6. The functional groups on the biochar surface are the adsorption centers. The adsorption enthalpy (ΔH) is always in the range of hydrogen bond energy. The weak interaction of the four adsorption configurations (A/B/C/D) is dominated by van der Waals forces and weak hydrogen bonds. The B configuration has the lowest binding energy and the most stable. The C configuration has the strongest weak interaction, and the D configuration is the weakest.
Key words: biocharphenoldensity functional theory (DFT)hydrogen bondvan der Waals force
苯酚是应用于石化、印染、医药等行业的基础工业原料[1],被列入全球优先控制污染物清单[2].利用吸附技术去除苯酚因成本低、效率高、易回收而得到广泛应用[3].生物炭是生物质在无氧或低氧条件下高温裂解碳化产生的富碳产物,孔隙结构发达,比表面积巨大,富含多种含氧官能团,吸附性能优异,在有机污染物控制领域潜力巨大[4].
严裕州等[5]利用NaOH改性荷梗生物炭,进行等温吸附、吸附动力学和共存离子竞争实验,探究其对苯酚的吸附机理,结果表明: 吸附机理为表面吸附/孔隙填充机制和π-π相互作用.张宁坤等[6]利用动力学、pH影响、等温吸附实验,发现生物炭对苯酚的吸附机理包括氢键作用、π-π作用和孔隙填充等.Teixidó等[7]研究发现生物炭对磺胺嘧啶的吸附机理包括磺胺嘧啶的苯环与生物炭表面的π-π作用和磺胺嘧啶的苯胺基、磺酰胺基与生物炭表面羧基或羟基间的氢键作用.上述研究有助于揭示生物炭与芳香族化合物间的吸附机理,但已有研究均基于模拟吸附实验数据、强化学键作用及经验推测,在微观(分子尺度)上缺乏直接证据,尤其缺乏芳香族化合物在生物炭表面(单分子层)弱相互作用机制的研究数据,因此不能获得涵盖全部微观作用的科学结论.
为了解决上述问题,本研究以苯酚为研究对象,利用量子化学密度泛函理论(density functional theory,DFT)[8],结合吸附实验和官能团表征等方法,探究生物炭和苯酚分子间的弱相互作用机制,研究结果将有助于完善生物炭与芳香族化合物间的相互作用理论.
1 材料与方法1.1 仪器与药品仪器: HZQ-F100振荡培养箱,哈尔滨市东联电子技术开发有限公司; DR6000紫外-可见分光光度计,哈希公司; 3H12RI智能高速冷冻离心机,湖南赫西仪器装备有限公司.
药品: 苯酚(分析纯),天津市大茂化学试剂厂; 稻壳生物炭(热解温度为400 ℃),天津亚德尔生物质科技股份有限公司.
1.2 吸附实验设计称取10 mg生物炭置于离心管中,向其加入10 mL质量浓度为10 mg/L的苯酚溶液,将溶液pH调至6.然后将离心管在25 ℃、200 r/min、避光条件下振荡72 h(基于动力学实验结果)后取出,在5 000 r/min下离心10 min,取上清液用紫外分光光度计(波长为269 nm)测量溶液中剩余苯酚质量浓度.
1.3 量子化学计算方法应用GaussView 5.0程序,构建生物炭表面分子结构、苯酚分子结构、生物炭与苯酚的吸附构型.应用Gaussian 09程序[9],采用密度泛函M06-2X/6-31+G(d, p)理论进行优化计算和频率分析,基于密度泛函M06-2X/6-311+G(d, p)理论计算单点能,并进行相应的BSSE(基组不完备性误差)校正,从而得到生物炭吸附苯酚的最低能量构型和相互作用能ΔEAB.ΔEAB=EAB-EA-EB.式中: ΔEAB为吸附构型的能量; EA为生物炭的能量; EB为苯酚的能量.
应用波函数分析程序Multiwfn[10],分析优化后的吸附构型的约化密度梯度(RDG)函数填色等值图探究弱相互作用的位置、类型及相对强度.分子中原子理论(AIM)分析是结合波函数分析程序Multiwfn对相互作用原子之间的键临界点(BCPS)进行搜索,得到键临界点(BCPS)处的拓扑参数(电子密度ρ、电子密度拉普拉斯值▽2ρ、拉格朗日动能G、势能电子密度V和能量密度H)并判断弱相互作用的类型及强度.
2 结果与讨论2.1 吸附实验结果与键能分析吸附动力学、关键参数(pH)影响和等温吸附实验结果见图 1. 结果表明,吸附初期(< 48 h)生物炭对苯酚的吸附速率较缓慢,随后对苯酚的吸附速率显著提升,到72 h时基本达到吸附平衡,吸附量q达到9.88 mg/g.吸附动力学可用拟一级动力学方程描述(图 1a).图 1b表明,吸附平衡时(72 h)体系的pH对吸附过程影响显著,整体呈先增后减的趋势,pH=6时,吸附效果最佳,pH>7时,吸附作用明显受到抑制,原因是在酸性和中性条件下,苯酚以分子形式存在于溶液中,与生物炭表面官能团接触充分,吸附效果较好; 而在碱性条件下,生物炭表面官能团和苯酚均解离为负离子状态,静电排斥作用大于吸引作用,吸附效果较差.图 1c表明,Freundlich拟合参数R2普遍比Langmuir拟合参数R2高,所以Freundlich等温吸附方程能够更好地描述生物炭对苯酚的吸附过程.
图 1(Fig. 1)
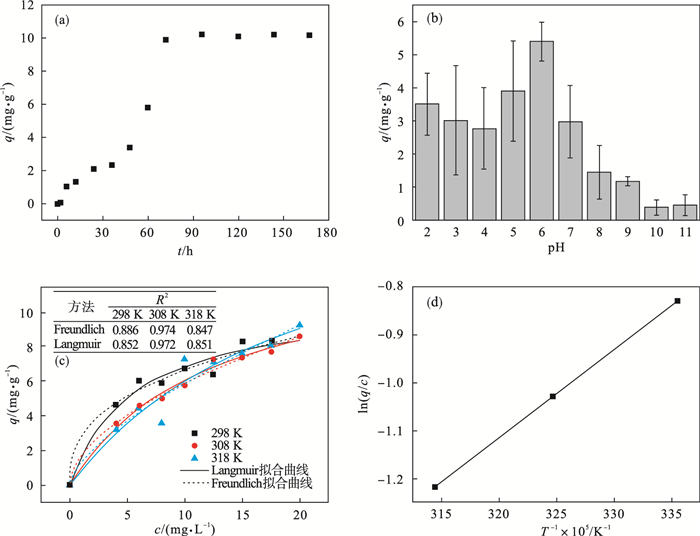 | 图 1 吸附实验结果Fig.1 Results of adsorption experiment (a)—吸附动力学;(b)—pH影响;(c)—等温吸附;(d)—ln(q/c)-1/T图. |
依据Van’t-Hoff方程[11-12],得
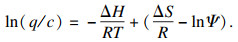 |
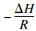
2.2 模型构象与红外表征通过红外表征分析生物炭吸附苯酚前后表面官能团变化(图 2).
图 2(Fig. 2)
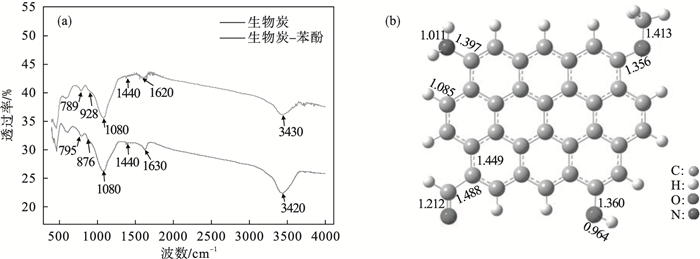 | 图 2 生物炭吸附苯酚前后的FT-IR图和生物炭构型Fig.2 FT-IR diagram of biochar before and after adsorption of phenol and biochar configuration (a)—FT-IR图;(b)—生物炭构型. |
由图 2a可知,在3 420 cm-1处存在—OH的吸收峰[14],在1 630 cm-1处存在芳香环中的C=C伸缩振动峰,在1 440 cm-1处存在C—H变形振动峰,在1 080 cm-1处存在C—O—C的吸收峰,在876 cm-1处存在N—H变形振动峰,在795 cm-1处存在=C—H面弯曲振动峰.吸收苯酚后,3 420 cm-1处的—OH吸收峰发生了蓝移,1 630 cm-1处的C=C伸缩振动峰发生了红移,876 cm-1处的N—H变形振动峰发生了蓝移,795 cm-1处的=C—H面弯曲振动峰发生了红移,说明生物炭表面的—OH,C=C,N—H,=C—H对吸附苯酚起到了作用.其中部分峰发生红移,说明生物炭表面官能团与苯酚可能形成氢键作用.
根据Qu等[15]的研究方法,结合生物炭FT-IR特征峰,推测表面官能团有—CHO,—OH,—NH2,—O—CH3.基于此,通过对多个芳香环的连接,搭建了具有10个芳香环的稠环结构,并用H原子对芳香环边缘进行补偿处理,用以描述生物炭结构.在稠环结构上枝接4种官能团,构成如图 2b所示的生物炭构型,作为后续探究弱相互作用的基本构型.
2.3 生物炭-苯酚吸附几何构型与结合能分析利用2.2节得到的生物炭构型,对苯酚与生物炭可能存在的几种吸附构型进行结构优化,并进行频率计算,得到如图 3所示的4种稳定构型.4种构型均为面对面平行的基面吸附构型,其中苯酚的—OH以4种方向分别与生物炭分子的4种官能团进行就近结合,可以看出苯酚分子与生物炭吸附位点在芳香环中心.
图 3(Fig. 3)
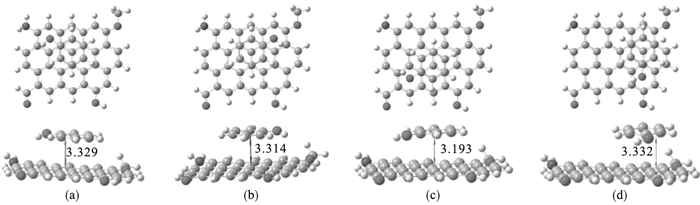 | 图 3 苯酚在生物炭表面的吸附构型Fig.3 Adsorption configuration of phenol on the surface of biochar (a)—A构型;(b)—B构型;(c)—C构型;(d)—D构型. |
由表 1可知,ΔH(实验)与H(隐式溶剂化,SMD)在数值上有一定差距,这是因为本研究所选用的生物炭热解温度较低,炭化程度不高,所以实验值比理论值低很多.隐式溶剂化下得到的吸附焓比理想气体状态(gas)下高,说明水环境有利于生物炭吸附苯酚.通过比较4种构型的吸附焓H(SMD)、吸附焓H(gas)和相互作用能E(BSSE),B构型能量最低最稳定.
表 1(Table 1)
| 表 1 吸附构型的结合能 Table 1 Binding energy of adsorption configuration |
2.4 约化密度梯度(RDG)分析RDG函数表达式:
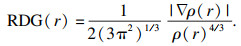 |
如图 4所示,苯酚与生物炭基面均存在范德华力对应的RDG等值面,说明存在范德华力,对应于散点图中分布在RDG值小于0.5 a.u.且sign(λ2)ρ值为零左右的区域内的散点.每个苯环中心均存在空间位阻等值面,表明存在空间位阻作用,对应于散点图中分布在RDG值小于0.5 a.u.,且sign(λ2)ρ值为0.02 a.u.左右的区域内的散点[16].如图 4所示,4个散点图中分布在sign(λ2)ρ值为-0.014 a.u.左右的区域内的散点代表弱氢键作用,说明苯酚与生物炭基面存在弱氢键作用.4种构型均存在范德华力作用和弱氢键作用,但4种构型中生物炭与苯酚间各官能团位置不同,使得弱相互作用位置和强度略有不同.
图 4(Fig. 4)
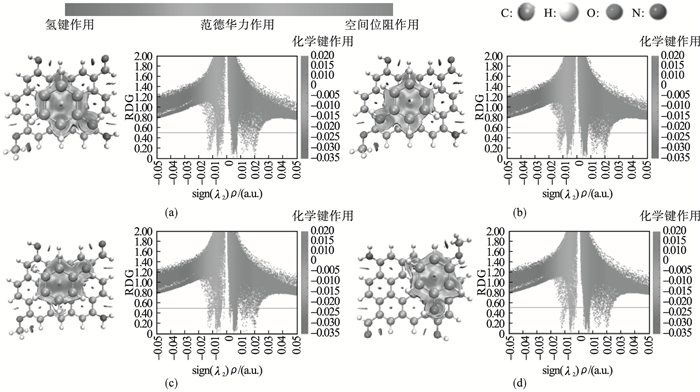 | 图 4 RDG等值面彩色图及散点图Fig.4 RDG isosurface color map and scatter plots (a)—A构型;(b)—B构型;(c)—C构型;(d)—D构型. |
2.5 分子中原子理论(AIM)分析对生物炭-苯酚间弱相互作用进行拓扑分析,如图 5所示.在4种吸附构型中,生物炭表面C原子与苯酚分子的C,O原子间存在拓扑路径,并且在路径中存在键临界点(BCPs).
图 5(Fig. 5)
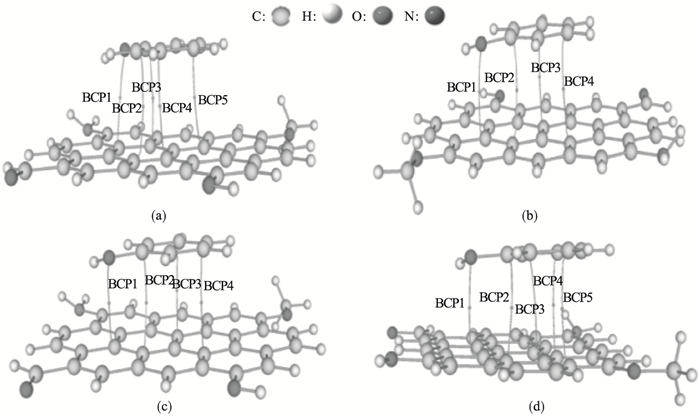 | 图 5 吸附构型的电子密度拓扑分析Fig.5 Topological analysis of electron density of adsorption configuration (a)—A构型;(b)—B构型;(c)—C构型;(d)—D构型. |
键临界点(BCPs)的拓扑参数如表 2所示.各键临界点处的电子密度的拉普拉斯值▽2ρ(BCP)均大于零,表明键临界点所对应的相互作用属于闭壳层相互作用[17].根据Cremer提出的准则[18],各键临界点处的|V(BCP)|<G(BCP)且H(BCP)>0,说明相互作用类型为非共价键作用.键临界点的电子密度ρ(BCP)与相互作用强度有关,其数值越高相互作用越强,因此C构型的弱相互作用最强,D构型最弱.
表 2(Table 2)
| 表 2 键临界点处电子密度的拓扑参数 Table 2 Topological parameters of the electron density at the critical point of the bond |
通过表 2可以看出各键临界点处的电子密度ρ(BCP)的数值在0.006 4~0.008 3之间,在区间[0.002 0.04]内,但其拉普拉斯值▽2ρ(BCP)在0.017~0.024之间,不完全在区间[0.02 0.15]内,不完全符合氢键判断标准[19].此外,氢键的强度可分为三类[20]: ①强氢键: V(BCP)+G(BCP)>0,▽2ρ(BCP) < 0; ②中氢键: V(BCP)+G(BCP) < 0,▽2ρ(BCP)>0; ③弱氢键: V(BCP)+G(BCP)>0,▽2ρ(BCP)>0.如表 2所示,各键临界点处的V(BCP)+G(BCP)>0,▽2ρ(BCP)>0.结合RDG分析,证明生物炭与苯酚分子间的弱相互作用介于范德华力作用和弱氢键作用之间.
3 结论1) 体系的pH对生物炭吸附苯酚影响显著,吸附72 h达平衡,吸附焓(ΔH)处于氢键键能范围内,表明生物炭-苯酚间的弱相互作用与氢键高度相关.
2) 生物炭表面官能团是吸附苯酚的作用中心,4种吸附构型中B构型结合能最低、最稳定,RDG分析表明4种吸附构型的氢键均为弱氢键,范德华力作用占主导.
3) AIM分析表明生物炭-苯酚间的弱相互作用机制为闭壳层作用中的范德华力作用和弱氢键作用,弱相互作用最强的是C构型,最弱的是D构型.
参考文献
| [1] | Busca G, Berardinelli S, Resini C, et al. Technologies for the removal of phenol from fluid streams: a short review of recent developments[J]. Journal of Hazardous Materials, 2008, 160(2/3): 265-288. |
| [2] | 仓金顺, 开启余, 陈瑜, 等. 水体中苯酚污染物的快速检测方法及测试盒研究[J]. 广东化工, 2014, 41(15): 261-262, 257. (Cang Jin-shun, Kai Qi-yu, Chen Yu, et al. Research on rapid detection method and test box of phenol pollutants in water[J]. Guangdong Chemical Industry, 2014, 41(15): 261-262, 257.) |
| [3] | 王玥. 突发水源苯酚污染给水应急处理技术研究[D]. 哈尔滨: 哈尔滨工业大学, 2013. (Wang Yue. Research on emergency treatment technology of water supply for sudden water source phenol pollution[D]. Harbin: Harbin Institute of Technology, 2013. ) |
| [4] | Zhu X, Li C, Li J, et al. Thermal treatment of biochar in the air/nitrogen atmosphere for developed mesoporosity and enhanced adsorption to tetracycline[J]. Bioresource Technology, 2018, 263: 475-482. DOI:10.1016/j.biortech.2018.05.041 |
| [5] | 严裕州, 王洁, 叶晓春, 等. NaOH改性荷梗生物炭的制备及对苯酚的吸附特性[J]. 武汉理工大学学报(信息与管理工程版), 2021, 43(3): 224-230. (Yan Yu-zhou, Wang Jie, Ye Xiao-chun, et al. Preparation of NaOH modified lotus stem biochar and its adsorption characteristics for phenol[J]. Journal of Wuhan University of Technology (Information and Management Engineering Edition), 2021, 43(3): 224-230. DOI:10.3963/j.issn.2095-3852.2021.03.005) |
| [6] | 张宁坤, 李潇川, 梁嘉莉, 等. 荷梗生物炭吸附突发苯酚污染研究[J]. 武汉理工大学学报(信息与管理工程版), 2021, 43(4): 302-308. (Zhang Ning-kun, Li Xiao-chuan, Liang Jia-li, et al. Study on the sudden phenol pollution of lotus stem biochar adsorption[J]. Journal of Wuhan University of Technology (Information and Management Engineering Edition), 2021, 43(4): 302-308. DOI:10.3963/j.issn.2095-3852.2021.04.002) |
| [7] | Teixidó M, Pignatello J J, Beltrán J L, et al. Speciation of the ionizable antibiotic sulfamethazine on black carbon(biochar)[J]. Environmental Science & Technology, 2011, 45(23): 10020-10027. |
| [8] | 陈玲, 林珍义, 肖瑶, 等. 氟代六元氮杂环化合物与水分子弱相互作用的理论研究[J]. 西华大学学报(自然科学版), 2021, 40(3): 98-104. (Chen Ling, Lin Zhen-yi, Xiao Yao, et al. Theoretical study on the weak interaction between fluorinated six-membered nitrogen heterocyclic compounds and water molecules[J]. Journal of Xihua University (Natural Science Edition), 2021, 40(3): 98-104.) |
| [9] | Frisch M J, Trucks G W, Schlegel H B, et al. Gaussian 09, Revision D. O1[Z]. Gaussian Inc, Wallingford CT, 2013. |
| [10] | Lu T, Chen F. Multiwfn: a multifunctional wavefunction analyzer[J]. Journal of Computational Chemistry, 2012, 33(5): 580-592. DOI:10.1002/jcc.22885 |
| [11] | Payne G F, Payne N N, Ninomiya Y, et al. Adsorption of non polar solutes onto neutral polymer sorbents[J]. Separation Science and Technology, 1989, 24: 457-465. DOI:10.1080/01496398908049782 |
| [12] | Payne G F, Ninomiya Y. Selective adsorption of solutes based on hydrogen bonding[J]. Separation Science and Technology, 1990, 25: 1117-1129. DOI:10.1080/01496399008051841 |
| [13] | 王庆文, 杨玉恒, 高鸿宾. 有机化学中的氢键问题[M]. 天津: 天津大学出版社, 1993: 1-243. (Wang Qing-wen, Yang Yu-heng, Gao Hong-bin. The hydrogen bond problem in organic chemistry[M]. Tianjin: Tianjin University Press, 1993: 1-243.) |
| [14] | Muhammad S U R, Kim I, Rashid N, et al. Adsorption of brilliant green dye on biochar prepared from lignocellulosic bioethanol plant waste[J]. Clean-Soil Air Water, 2016, 44(1): 55-62. DOI:10.1002/clen.201300954 |
| [15] | Qu Z B, Sun F, Liu X, et al. The effect of nitrogen-containing functional groups on SO2 adsorption on carbon surface: enhanced physical adsorption interactions[J]. Surface Science, 2018, 677: 78-82. DOI:10.1016/j.susc.2018.05.019 |
| [16] | Xu H, Chu W, Huang X, et al. CO2 adsorption-assisted CH4 desorption on carbon models of coal surface: a DFT study[J]. Applied Surface Science, 2016, 375: 196-206. DOI:10.1016/j.apsusc.2016.01.236 |
| [17] | Carroll M T, Bader R F. An analysis of the hydrogen bond in BASE-HF complexes using the theory of atoms in molecules[J]. Molecular Physics, 1988, 65(3): 695-722. DOI:10.1080/00268978800101351 |
| [18] | Espinosa E, Alkorta I, Elguero J, et al. From weak to strong interactions: a comprehensive analysis of the topological and energetic properties of the electron density distribution involving X-H, …, F-Y systems[J]. The Journal of Chemical Physics, 2002, 117(12): 5529-5542. |
| [19] | Alabugin I V, Manoharan M, Peabody S, et al. Electronic basis of improper hydrogen bonding: a subtle balance of hyperconjugation and rehybridization[J]. Journal of the American Chemical Society, 2003, 125(19): 5973-5987. |
| [20] | Rozas I, Alkorta I, Elguero J. Behavior of ylides containing N, O, and C atoms as hydrogen bond acceptors[J]. Journal of the American Chemical Society, 2000, 122: 11154-11161. |