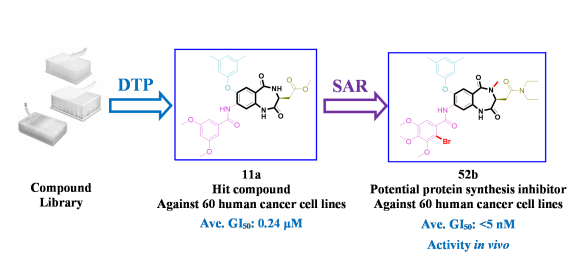
基于表型筛选化合物库确定了苗头化合物11a,SAR研究得到化合物52b
刘刚团队通过与美国国家癌症中心(National Cancer Institute)的长期合作,对课题组内的“优势骨架导向性”化合物库进行基于抑制癌细胞生长表型的活性筛选,发现了两类具有抗肿瘤活性的化合物,一类为苯并噻唑类衍生物,另一类为1,4-苯并二氮杂卓-2,5-二酮衍生物。进一步对1,4-苯并二氮杂卓-2,5-二酮苗头化合物11a深入的“构-效”关系研究,发现了具有广谱抗癌活性的化合物52b,其对9类60株人癌细胞的平均50%生长抑制浓度(GI50)小于5nM,具体“构-效”关系总结如下。
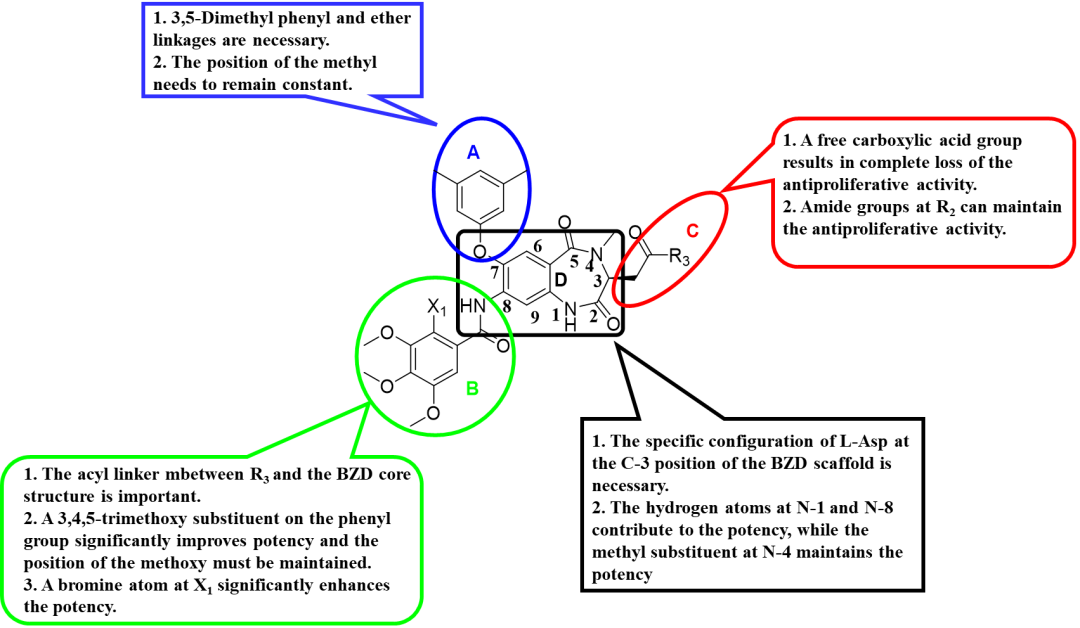
1,4-苯并二氮杂卓-2,5-二酮类化合物的抗肿瘤活性“构-效”关系
机制研究表明,化合物52b可将肿瘤细胞生长阻滞在G1/S期,并诱导细胞凋亡家族蛋白活化。通过NCI correlation coefficients(COMPARE analysis)分析及相应的实验研究,排除了化合物作为微管蛋白抑制剂、拓扑异构酶抑制剂、以及激酶抑制剂的可能性。
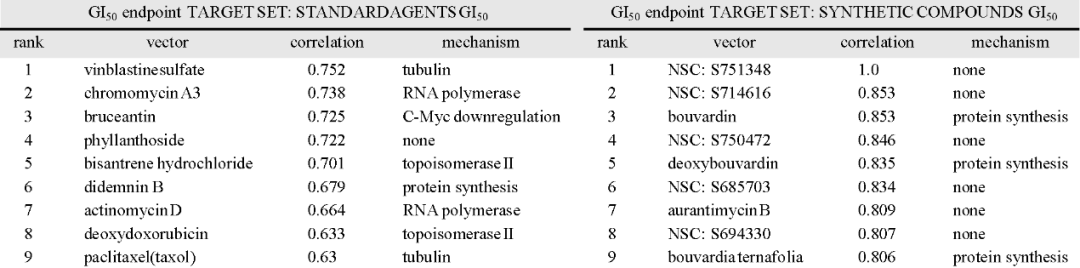
COMPARE分析预测化合物潜在作用机制
进一步研究发现,化合物52b可有效抑制癌基因c-Myc的蛋白表达,但并不影响c-Myc的转录。Polysome profile分析表明该化合物通过阻止多聚核糖体的形成,抑制细胞内蛋白质的合成。体内实验表明该化合物可有效抑制NCI-H522肺癌裸鼠移植瘤模型的肿瘤生长。
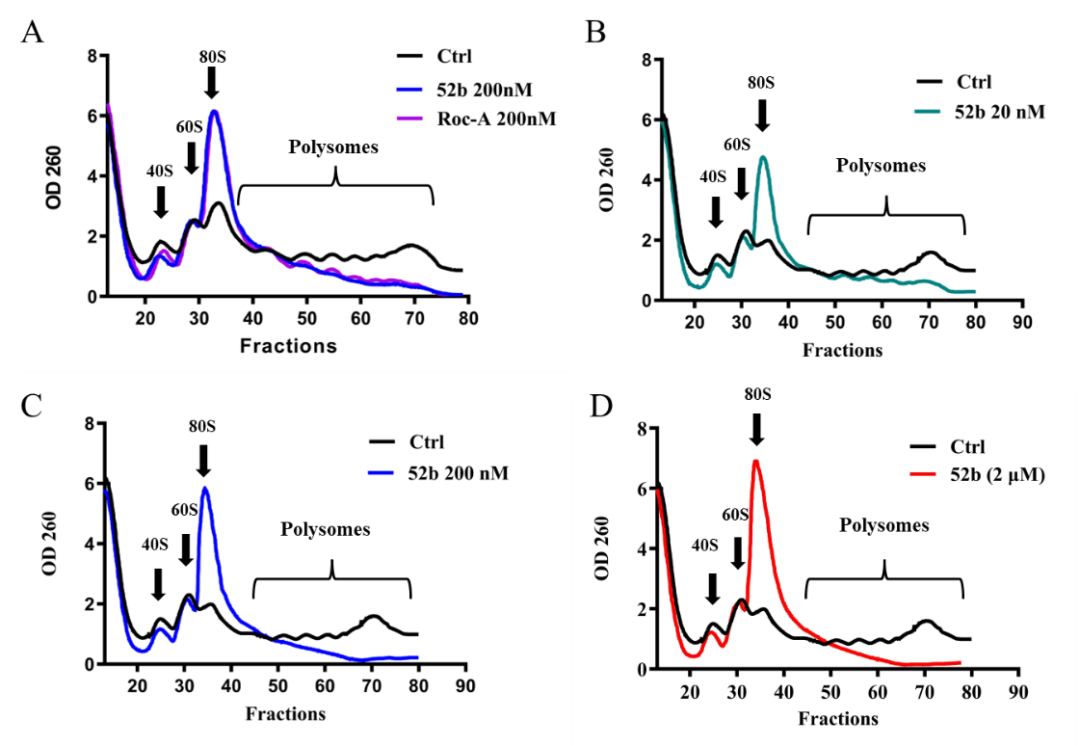
Polysome profile分析显示化合物52b抑制多聚核糖体的形成
综上所述,该研究通过构建“优势骨架导向性”化合物库,结合基于表型的大规模活性筛选及药物化学优化手段,发现了具有超高抗肿瘤活性的化合物52b,该化合物通过抑制多聚核糖体的形成,抑制肿瘤相关蛋白的表达,进而诱导肿瘤细胞凋亡。
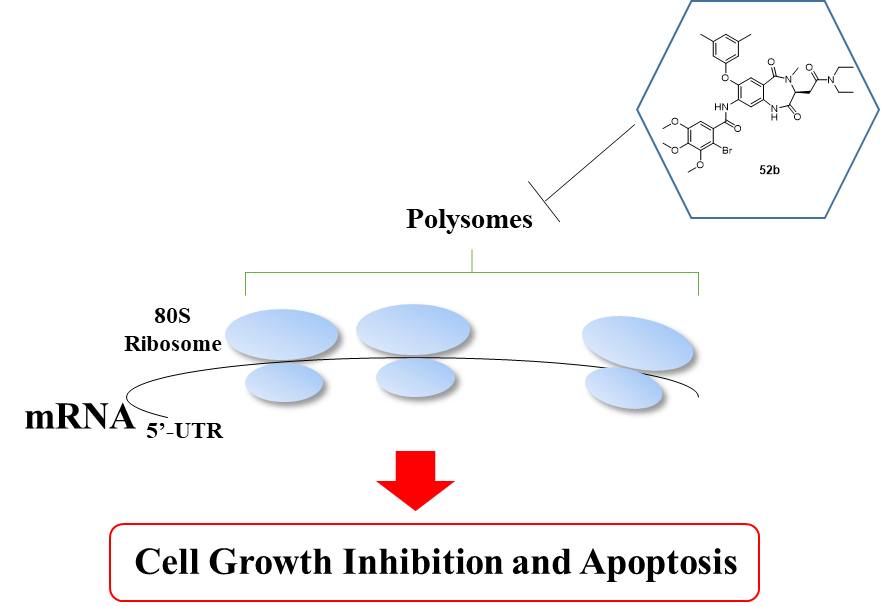
化合物52b的抗癌活性作用机制假想图
本项研究工作在线发表于美国化学会《药物化学期刊》(Journal of Medicinal Chemistry),题为“一类具有高效抗癌活性的1,4-苯并二氮杂卓衍生物作为潜在蛋白质合成抑制剂的发现”(Identification of 1,4-Benzodiazepine-2,5-dione Derivatives as Potential Protein Synthesis Inhibitors with Highly Potent Anticancer Activity)。
清华大学药学院刘刚教授及中国医学科学院药物研究所董毅副研究员为本文的通讯作者。刘刚课题组于文俊博士、解希雷博士、马瑶博士为本论文的共同第一作者。本项研究得到了国家自然科学基金委以及清华-佛山创新专项基金的支持和帮助。
论文链接:
https://pubs.acs.org/doi/10.1021/acs.jmedchem.2c01431
供稿:药学院
题图设计:任帅
编辑:李华山
审核:吕婷
2022年10月28日 08:17:57
