8月5日,清华大学化学系副教授刘凯、张洪杰院士团队在《科学·进展》(Science Advances)期刊发表了题为“活细胞内高靶专一性和高鲁棒性的数字信息分子级处理系统”(In vivo processing of digital information molecularly with targeted specificity and robust reliability)的研究论文。文章展示,在大肠杆菌活细胞内,文字、密码表、图片等信息可以被长期稳定的存储、修改和复制,并开发了一种双质粒编辑系通用于准确处理微生物载体中的数字信息。
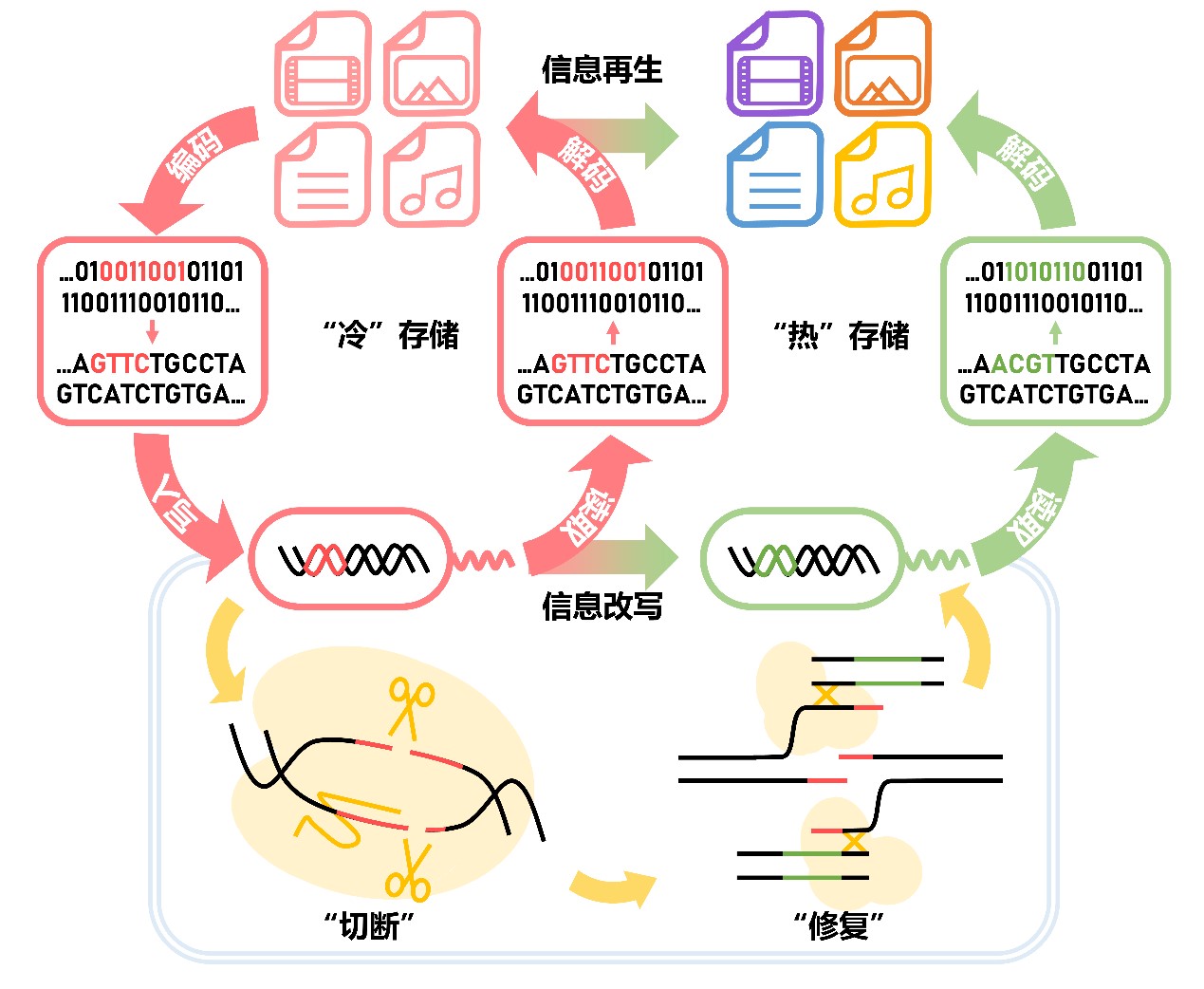
研究团队建立的活细胞DNA数字信息存储与改写系统
研究人员通过利用CRISPR/Cas基因编辑技术,在活细胞中构建了集存储与改写功能于一体的双质粒信息存储体系,与已有的DNA信息存储方式相比,在降低写入信息冗余度、提高活细胞信息存储能力、简化信息读取流程、提升信息保存安全性上都有显著提升。该研究充分探索了DNA序列的编码能力,不需要任何寻址索引和备份序列,并兼容多种编码算法,最高的编码效率可达每个核苷酸4.0位(4.0bits/nucleotide)。
值得注意的是,该研究设计的信息存储与定点修改技术,不仅可以利用活细胞对外源数字信息实现高密度存储和稳定拷贝,还能利用活细胞内的蛋白质工具实现灵活的信息处理。利用预设并优化的CRISPR-Cas12a体系导向crRNA结合序列,可以实现与现有基因编辑相媲美的编辑成功率,并完成在分子水平精准靶向多种类型复杂信息的信息修改处理目标。另外,创新性引入荧光蛋白作为“报告器”进一步使信息改写可视化,极大地提高了改写信息的读取鲁棒性,使分子水平信息存储和修改的状态直观可见。这一研究解决了DNA作为存储介质无法对大数据信息进行精准改写的难点,克服了DNA基质只能作为冷数据存储的弊端,提升了DNA作为信息热存储介质的能力。
清华大学化学系为第一完成单位,化学系2020级博士研究生刘杨奕为论文第一作者,清华大学化学系副教授刘凯为通讯作者。清华大学化学系张洪杰院士和上海交通大学樊春海院士给予了大力指导,研究得到了国家自然科学基金、科技部重点研发计划、清华大学春风基金的支持。
论文链接:
https://www.science.org/doi/10.1126/sciadv.abo7415
供稿:化学系
题图设计:金娅辰
编辑:李华山
审核:郭玲 吕婷
2022年08月11日 08:59:00
