 , 朱维晃1,2
, 朱维晃1,2
 , 郑飞1,2, 文虎1,2
, 郑飞1,2, 文虎1,21. 西安建筑科技大学, 陕西省环境工程重点实验室, 西安 710055;
2. 西安建筑科技大学, 西北水资源与环境生态教育部重点实验室, 西安 710055
收稿日期: 2018-04-18; 修回日期: 2018-06-06; 录用日期: 2018-06-06
基金项目: 国家自然科学基金(No.41373093)
作者简介: 李云姣(1993-), 女, E-mail:1508041742@qq.com
通讯作者(责任作者): 朱维晃, E-mail:zhuweihuang@xauat.edu.cn
摘要: 在希瓦氏菌(Shewanella putrefaciens)呼吸驱动下,成功制备了生源性还原态的氧化石墨烯(r-GO)修饰的碳毡电极,进一步研究了r-GO修饰碳毡电极与微生物相互作用的电化学特征.结果表明:经r-GO修饰的碳毡电极与微生物的相互作用程度得到显著提升,这主要是由于修饰后电极的扩散内阻(Rdif)得到快速降低的结果.将r-GO修饰后的碳毡电极作为阳极应用于微生物燃料电池(MFC)中,经微生物呼吸驱动下的石墨烯修饰电极,由于Rdif降低导致电极的电化学活性增强,使得电极和微生物相互作用程度得到提升,从而缩短了MFC启动时间,提高了MFC的产电能力.研究进一步表明,r-GO对电极的修饰,调控了对电极电化学活性及生源性电子向电极表面的传递过程.
关键词:石墨烯电极修饰微生物-电极相互作用
Electrochemical characteristics of the interaction between graphene modified carbon felt electrode and microbe
LI Yunjiao1,2
 , ZHU Weihuang1,2
, ZHU Weihuang1,2
 , ZHENG Fei1,2, WEN Hu1,2
, ZHENG Fei1,2, WEN Hu1,2 1. Shaanxi Key Laboratory of Environmental Engineering, Xi'an University of Architecture and Technology, Xi'an 710055;
2. Key Laboratory of Northwest Water Resource, Environment and Ecology, MOE, Xi'an University of Architecture and Technology, Xi'an 710055
Received 18 April 2018; received in revised from 6 June 2018; accepted 6 June 2018
Supported by the National Natural Science Foundation of China (No.41373093)
Biography: LI Yunjiao(1993—), female, E-mail:1508041742@qq.com
*Corresponding author: ZHU Weihuang, E-mail:zhuweihuang@xauat.edu.cn
Abstract: The carbon felt electrode modified by microbially reduced graphene oxide (r-GO) was successfully prepared during the respiration process of Shewanella putrefaciens, and the electrochemical characteristics of the interaction between r-GO modified carbon felt electrode and microbe were studied. The results show that the interaction between the r-GO modified carbon felt electrode and the microbe is enhanced significantly, mainly due to the rapid decrease of the diffusion resistance (Rdif) of the r-GO modified electrode. The r-GO modified carbon felt electrode was further used as anode in microbial fuel cell (MFC), subsequently, the start-up of MFC was shortened and MFC performance was improved. The research indicates that the electrode modification with r-GO could regulate the electrode electrochemical activity and the electron transfer process between microbe and electrode.
Keywords: grapheneelectrode modificationmicrobe-electrode interaction
1 引言(Introduction)在限制微生物燃料电池(MFC)运行的众多因素中, 电极特别是生物阳极的电化学活性是不容忽视的一个重要因素(Logan et al., 2012).因此, 如何改善阳极的电化学活性是强化MFC产电能力的关键.关于改善阳极电化学活性的相关研究, 大多是对阳极材料进行修饰或改性(刘中良等, 2014;Liu et al., 2014;Cui et al., 2015), 以利于阳极表面形成高电化学活性生物膜, 促进胞外电子转移(EET).其中, 石墨烯(graphene)作为碳纳米材料, 由于具有优良的物理化学性能(Stoller et al., 2008;Zhang et al., 2010), 将其应用于修饰阳极材料已引起人们的关注(Guo et al., 2014;Song et al., 2016;陈洁等, 2016).目前, 已有利用化学粘合剂如聚四氟乙烯等将石墨烯负载在阳极材料的报道(Li et al., 2012), 但粘合剂会降低电极的表面积和导电性.Zhang等(2016)将阳极材料浸泡在氧化石墨烯(Graphene Oxide, GO)悬浮液中, 之后利用电化学还原GO为还原态氧化石墨烯(r-GO), 作为MFC阳极提高产电效果, 但这种浸泡负载石墨烯的方法易出现石墨烯脱落的现象.另有研究表明, 从反应体系接种到微生物在阳极顺利固着, 需要长达几十天才能形成成熟的生物膜(Zhao et al., 2015).
因此, 寻求一种有效修饰阳极的方法并使得微生物和阳极之间的EET过程得以顺利进行, 受到越来越多的关注(薛丽仙等, 2016;黄力华等, 2017).基于此, 本文利用微生物呼吸作用驱动, 成功制备了生源性还原态氧化石墨烯(r-GO)修饰的碳毡电极, 对修饰及未修饰阳极分别进行循环伏安(CV)、交流阻抗(EIS)及电流-时间(i-t)等电化学响应特征分析, 并考察修饰/未修饰电极与微生物相互作用的特征, 以及GO修饰后碳毡电极作为阳极对MFC性能的影响.以期为电极与微生物相互作用过程的机制与特征研究提供有益的理论参考与建议.
2 材料和方法(Materials and methods)2.1 r-GO修饰碳毡电极的制备菌液培养:将Shewanella putrefaciens菌液接种到灭菌后的LB培养基中, 在120 r·min-1的37 ℃恒温振荡培养箱中培养, 至吸光度OD600=1.0.然后将菌液离心, 将底部菌体重悬浮于100 mL含5%LB培养基和95%乳酸钠(18 mmol·L-1)的M9培养液.LB培养基成分为:3 g·L-1牛肉膏、10 g·L-1蛋白胨和5 g·L-1 NaCl, 用NaOH溶液调节培养基pH至7.0左右.M9成分为:6 g·L-1 Na2HPO4、3 g·L-1 KH2PO4、0.5 g·L-1 NaCl、1 g·L-1 NH4Cl、1 mmol·L-1 MgSO4和0.1 mmol·L-1 CaCl2.
r-GO修饰碳毡电极的制备:氧化石墨烯(Graphene Oxide, GO)根据Hummers方法制备而成(Jr et al., 1958).将11 mL浓度为1 g·L-1的氧化石墨烯悬浮液于上述100 mL菌悬浮液混合均匀, 最终配成GO浓度为0.1 g·L-1的氧化石墨烯-微生物混合液.将经10%过氧化氢处理的碳毡电极(1 cm×2 cm)浸没于氧化石墨烯-微生物混合液中, 再以铂片为对电极, Ag/AgCl (sat. KCl)作为参比电极, 组建三电极单室反应器.在微生物呼吸作用的驱动下, GO被还原为r-GO并附着在碳毡电极表面, 完成对碳毡电极的r-GO的自发修饰过程.
2.2 电化学分析与测试以一定的时间间隔进行CV和EIS测定分析.CV测定及施加恒电位+0.1 V(vs Ag/AgCl)步骤在电化学工作站(上海辰华CHI 660)上进行;交流阻抗(EIS)测试在普林斯顿(USA, Princeton 2273)电化学工作站上进行.电流-时间(i-t)、循环伏安曲线(CV)和电化学阻抗(EIS)均采用三电极体系, 阳极电极作为工作电极, 铂电极为对电极, Ag/AgCl (sat. KCl)作为参比电极.其中, CV测试的电压扫描范围为-0.7~0.7 V, 扫描速率为10 mV·s-1.EIS测试频率范围为100 kHz~10 mHz.MFC产电特征利用数据采集卡以1 min每次的频率监测开路电压和750 Ω外电阻的电压.
2.3 双室MFC的构建与运行每组双室MFC体系由阳极室和阴极室构成, 两组体系阳极室电极分别为r-GO/CF阳极和CF阳极, 阴极室电极均为铂片电极.双室内溶液体积各为130 mL, 阳极室与阴极室用质子交换膜分开.阳极液为M9培养液(6 g· L-1Na2HPO4、3 g·L-1 KH2PO4、0.5 g·L-1NaCl、1 g·L-1 NH4Cl、1 mmol·L-1 MgSO4、0.1 mmol·L-1 CaCl2), 阴极液为50 mmol·L-1 K3[Fe(CN)6]和50 mmol·L-1 KCl.阳极通入氮气15 min后, 密封.MFC体系装置在32 ℃条件下, 外接750 Ω电阻.
2.4 SEM电镜表征扫描电子显微镜(SEM)形貌表征:将1 cm×1 cm左右的电极在2.5%的戊二醛溶液(用0.1 mol·L-1磷酸盐缓冲溶液配制)中完全浸泡24 h, 保鲜膜封口, 然后依次用25%、50%、75%、85%、95%和100%的乙醇梯度脱水, 每次10 min, 取出室温干燥, 将干燥后的电极喷金后电镜观察.
3 结果和讨论(Results and discussion)3.1 微生物-电极之间的电子转移特征含经r-GO修饰后电极(r-GO/CF)的反应体系中, 在经历约20 h后, 因微生物呼吸产生的电子定向传递给电极而形成生源性电流的过程得以启动, 在58 h时电流可达0.185 mA(图 1).这主要是因为石墨烯具有良好的导电性能和巨大的比表面积, 吸附包裹了大量的菌体, 附着在经r-GO修饰的碳毡电极表面(图 2b), 从而使得微生物和电极之间的电子传递过程更易进行.对于未修饰碳毡电极(CF)的体系, 在整个实验阶段, 电流均远低于含r-GO/CF电极体系.表明未经r-GO修饰的CF, 菌体难以有效接触电极(图 2c~2d), 微生物和电极之间的电子传递过程没有得到有效构建, 与含r-GO修饰电极的体系相比, 其生源性电流强度得到显著降低.
图 1(Fig. 1)
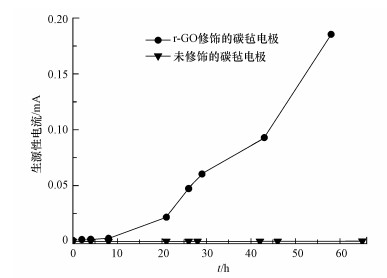 |
| 图 1 反应体系中微生物产电特征 (工作电极施加+0.1 V(vs Ag/AgCl)) Fig. 1The exoelectrogenic characteristics of the systems (The working electrodes were poised at a potential of +0.1 V(vs Ag/AgCl)) |
图 2(Fig. 2)
 |
| 图 2 r-GO修饰的碳毡电极(a, b)和未修饰碳毡电极(c, d)的扫描电镜(SEM)图 Fig. 2SEM images of the r-GO modified carbon felt electrode (a, b) and the unmodified carbon felt electrode (c, d) |
3.2 微生物-电极之间相互作用的电化学特征3.2.1 循环伏安法分析循环伏安法(CV)可用来表征电极的生物电催化活性(Babauta et al., 2012).根据CV测试结果可计算出发生在电极表面的电荷转移量(Q), 可由公式给出:
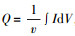
未修饰的碳毡(CF)电极在CV测试过程中的电流响应值(I)微弱, 在不同反应时间均不超过0.06 mA(图 3a), 而CF电极经r-GO修饰后电化学活性增强, 其电流响应值(I)得到显著提升(图 3b), 发生在电极表面的电荷转移量(Q)也随之增加(图 4), 在反应经58 h后, Q值接近0.2 C;而未修饰的CF电极的电荷转移量始终维持在约0.0025 C的较低水平, 约是r-GO修饰电极的1.25%左右.以上结果表明, 微生物呼吸过程中积累的电子能高效快速传递至r-GO修饰后的碳毡电极表面, 而上述传递过程在未修饰碳毡表面则得到明显抑制(图 4).
图 3(Fig. 3)
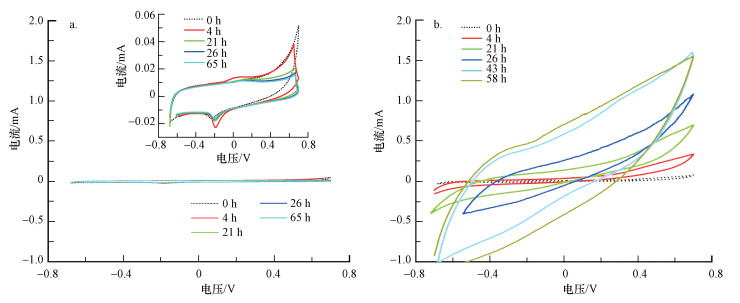 |
| 图 3 不同反应时间反应体系的循环伏安(CV)测试曲线 (a.未修饰的碳毡电极(CF), b.r-GO修饰的r-GO/CF电极) Fig. 3Cyclic voltammetry of electrode after different reaction time (a. the unmodified carbon felt electrode, b.the r-GO modified carbon felt electrode) |
图 4(Fig. 4)
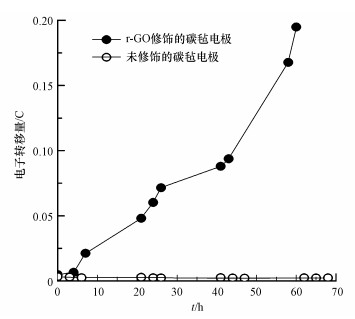 |
| 图 4 发生在微生物-电极之间的电子转移量 Fig. 4The quantity of electron transferred between microbe and electrode |
3.2.2 交流阻抗(EIS)分析对于电极-微生物相互作用的研究而言, EIS分析测试手段主要用于表征电极表面的电子传递过程的难易程度(Manohar et al., 2008), 常被关注的3个参数分别为溶液内阻(Rs)、电极表面电荷传递内阻(Rct)、反应物由溶液本体向电极表面扩散内阻(Rdif).
基于等效电路模型(Rs(QRct)(QRdif)), 其中, Q为等效常相位角元件, 将EIS测试结果用ZSimpWin软件拟合, 结果见图 5a和图 6a.溶液内阻Rs表示反应组成的本身性质, 其值基本不变.对于r-GO修饰后的r-GO/CF电极, 其Rct数值在约400~1100 Ω范围内波动, 反应前期有增加趋势, 在后期第58 h时, 恢复至反应初期水平(图 5b).其变化趋势可能反映了微生物驱动下的r-GO对碳毡电极的修饰过程中的动态变化情况.对于未修饰的碳毡电极CF来说, Rct变化情况也不明显, 维持在约400 Ω附近(图 6b).
图 5(Fig. 5)
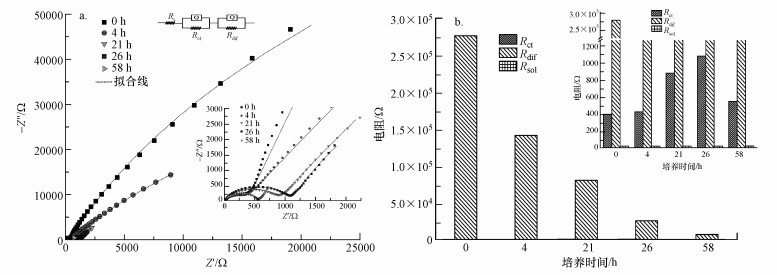 |
| 图 5 r-GO/CF电极的交流阻抗(EIS)测定与拟合结果(a)及拟合参数(b) Fig. 5EIS of the r-GO/CF electrode and the curve fitting with equivalent current (a) and fitting parameter (b) |
图 6(Fig. 6)
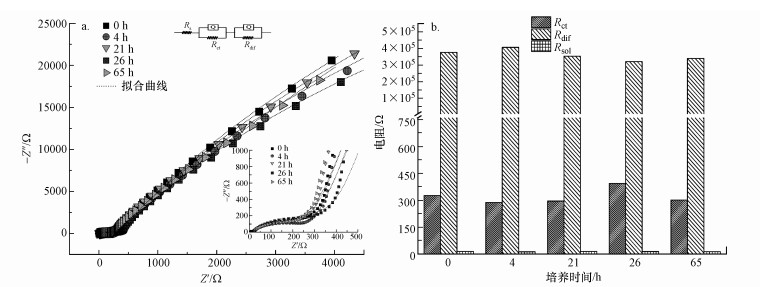 |
| 图 6 未修饰CF电极的交流阻抗(EIS)测定与拟合结果(a)及拟合参数(b) Fig. 6EIS of the unmodified CF electrode and fitting result (a) and fitting parameter (b) |
经石墨烯修饰r-GO/CF电极的扩散内阻Rdif变化值十分显著, 由反应初期的2.76×105 Ω减小至第58 h时的7341 Ω, 约降低了97.3%(图 5b), 同时, 微生物-电极之间的电子转移量也随之得到显著提升(图 4).未修饰的CF电极的Rdif在反应末期仍维持在3.5×105 Ω左右(图 6b), 远高于反应末期r-GO/CF电极的Rdif, 虽然Rct也有小幅波动, 与含r-GO/CF电极的体系类似, 但发生电极-微生物界面的电子转移量十分微弱(图 4).
经r-GO修饰后的电极表面积增加, 对电解质的吸附容量也相应增加, 故电极表面因吸附而富集的反应物浓度较本体溶液高, 减弱了传质过程中的浓度控制因素, 从而使得反应物更易由溶液本体向电极表面扩散(Hauch et al., 2001;Dao et al., 2018), 因此, 反应物由溶液本体向电极表面扩散内阻(Rdif)得到降低.
由于修饰后的r-GO/CF电极的Rdif显著降低, 微生物代谢过程中必须的生源要素由溶液本体向电极表面扩散更易进行, 有利于微生物的代谢过程, 从而强化了微生物-电极之间的相互作用和电子转移过程(图 1和图 4).基于以上结果并结合图 5b和图 6b, 可知电极表面扩散内阻即Rdif的大小是电极与微生物相互作用过程的主控因素, r-GO修饰作用是碳毡(CF)电极的Rdif得到显著降低的原因.
为进一步考察r-GO修饰过程的作用, 反应约70 h后, 将体系电解液中GO去除, 终止r-GO对碳毡电极的修饰过程.结果表明, r-GO修饰碳毡电极过程终止后, 电极的电荷转移内阻Rct由修饰中的461 Ω增加至1488 Ω(图 7), 而Rdif也上升至2.1×106 Ω.表明r-GO对电极的修饰过程, 调控了对电极的电化学活性及生源性电子向电极表面传递过程.
图 7(Fig. 7)
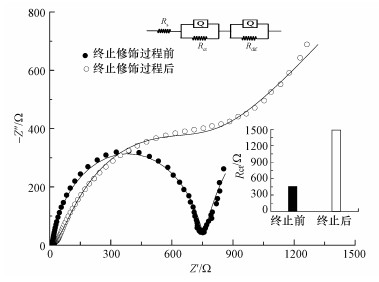 |
| 图 7 r-GO/CF电极的交流阻抗(EIS)测定与拟合结果及拟合参数 Fig. 7EIS of the r-GO/CF electrode and fitting result and fitting parameter |
3.3 不同电极组装的MFC产电分析开路电压(OCP)为阴极(Cathode)与阳极(Anode)的电势差, 即OCP=Ecathode-Eanode, Ecathode由阴极室电解液铁氰化钾浓度决定, 本实验中其浓度恒定为50 mmol·L-1.作为阳极的碳毡随着r-GO修饰过程的进行, 微生物在阳极表面聚集, 伴随着微生物的呼吸作用产生电子, Eanode逐渐降低, 因此, OCP不断增加, 在10 h后可达0.72 V左右.而采用未修饰碳毡为阳极的MFC的开路电压基本保持在0.15 V左右(图 8a).对于MFC闭路电压(串联外电阻750 Ω)也体现出类似的特征, 即以r-GO修饰后的r-GO/CF电极为阳极的MFC闭路电压峰值可达0.178 V, 而对于未修饰的以CF为阳极的MFC闭路电压峰值为0.111 V(图 8b).以上数据表明碳毡电极经r-GO修饰后, 电极的电化学活性得到增强, 促进了微生物在其表面的呼吸作用, 从而缩短MFC启动时间, 提高了MFC的产电能力.
图 8(Fig. 8)
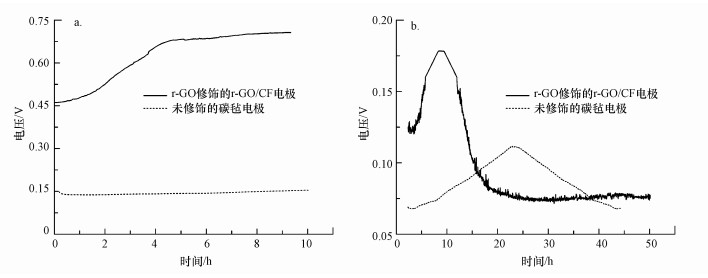 |
| 图 8 运行MFC过程所采集的电压 (a.开路电压, b.闭路电压) Fig. 8The voltage output of the MFC (a. open circuit potential, b.closed circuit potential) |
4 结论(Conclusions)1) 在Shewanella putrefaciens呼吸驱动下, 成功制备了还原态氧化石墨烯(r-GO)修饰的碳毡电极, 使得微生物和电极之间的电子传递过程得到有效构建.
2) 碳毡电极经r-GO修饰后, 电极的生物电化学活性得到显著提升.微生物-电极之间的电子传递过程中的生源性电流可达0.185 mA.微生物呼吸过程中积累的电子能高效快速传递至r-GO修饰后的碳毡电极表面, 而上述传递过程在未修饰碳毡表面则受到明显抑制.
3) 电极表面扩散内阻(Rdif)是电极与微生物相互作用过程的主控因素, r-GO修饰作用是碳毡(CF)电极的Rdif得到显著降低的原因.
参考文献
| Babauta J, Renslow R, Lewandowski Z, et al. 2012. Electrochemically active biofilms:facts and fiction.A review[J]. Biofouling, 28(8): 789–812.DOI:10.1080/08927014.2012.710324 |
| 陈洁, 孙健, 胡勇有. 2016. 石墨烯修饰电极微生物燃料电池及其抗菌性研究进展[J]. 环境科学学报, 2016, 36(2): 387–397. |
| Cui H F, Du L, Guo P B, et al. 2015. Controlled modification of carbon nanotubes and polyaniline on macroporous graphite felt for high-performance microbial fuel cell anode[J]. Journal of Power Sources, 283: 46–53.DOI:10.1016/j.jpowsour.2015.02.088 |
| Dao V D, Choi H S. 2018. Balance between the charge transfer resistance and diffusion impedance in a CNT/Pt counter electrode for highly efficient liquid-junction photovoltaic devices[J]. Organic Electronics, 58: 159–166.DOI:10.1016/j.orgel.2018.03.046 |
| Fricke K, Harnisch F, Schr?der U. 2008. On the use of cyclic voltammetry for the study of anodic electron transfer in microbial fuel cells[J]. Energy & Environmental Science, 1(1): 144–147. |
| Guo W, Cui Y R, Song H, et al. 2014. Layer-by-layer construction of graphene-based microbial fuel cell for improved power generation and methyl orange removal[J]. Bioprocess Biosyst Eng, 37(9): 1749–1758.DOI:10.1007/s00449-014-1148-y |
| Hauch A, Georg A. 2001. Diffusion in the electrolyte and charge-transfer reaction at the platinum electrode in dye-sensitized solar cells[J]. Electrochim Acta, 46(22): 3457–3466.DOI:10.1016/S0013-4686(01)00540-0 |
| 黄力华, 李秀芬, 任月萍, 等. 2017. 石墨烯掺杂聚苯胺阳极提高微生物燃料电池性能[J]. 环境科学, 2017, 38(4): 1717–1725. |
| Jr W S H, Offeman R E. 1958. Preparation of Graphitic Oxide[J]. Journal of the American Chemical Society, 80(6): 1339–1339.DOI:10.1021/ja01539a017 |
| Li X L, Song H F, Wang H, et al. 2012. A nanocomposite of graphene/MnO2 nanoplatelets for high-capacity lithium storage[J]. Journal of Applied Electrochemistry, 42(12): 1065–1070.DOI:10.1007/s10800-012-0488-z |
| Liu J, Liu J F, He W H, et al. 2014. Enhanced electricity generation for microbial fuel cell by using electrochemical oxidation to modify carbon cloth anode[J]. Journal of Power Sources, 265(4): 391–396. |
| 刘中良, 周宇, 侯俊先, 等. 2014. 活性炭修饰微生物燃料电池阳极的研究[J]. 水处理技术, 2014(4): 16–18. |
| Logan B E, Rabaey K. 2012. Conversion of wastes into bioelectricity and chemicals by using microbial electrochemical technologies[J]. Science, 337(6095): 686–690.DOI:10.1126/science.1217412 |
| Manohar A K, Bretschger O, Nealson K H, et al. 2008. The use of electrochemical impedance spectroscopy (EIS) in the evaluation of the electrochemical properties of a microbial fuel cell[J]. Bioelectrochemistry, 72(2): 149–154.DOI:10.1016/j.bioelechem.2008.01.004 |
| Song R B, Zhao C E, Jiang L P, et al. 2016. Bacteria-affinity 3D macroporous graphene/MWCNTs/Fe3O4 foams for high-performance microbial fuel cells[J]. ACS Applied Materials & Interfaces, 8(25): 16170–16177. |
| Stoller M D, Park S, Zhu Y, et al. 2008. Graphene-based ultracapacitors[J]. Nano Letters, 8(10): 3498–3502.DOI:10.1021/nl802558y |
| 薛丽仙, 杨娜, 任月萍, 等. 2016. 石墨烯掺杂生物阳极微生物燃料电池的产电性能[J]. 环境化学, 2016, 35(5): 1014–1019. |
| Zhang C Y, Liang P, Yang X F, et al. 2016. Binder-free graphene and manganese oxide coated carbon felt anode for high-performance microbial fuel cell[J]. Biosensors and Bioelectronics, 81: 32–38.DOI:10.1016/j.bios.2016.02.051 |
| Zhang L L, Zhou R, Zhao X S. 2010. Graphene-based materials as supercapacitor electrodes[J]. Journal of Materials Chemistry, 20(29): 5983–5992.DOI:10.1039/c000417k |
| Zhao S L, Li Y C, Yin H J, et al. 2015. Three-dimensional graphene/Pt nanoparticle composites as freestanding anode for enhancing performance of microbial fuel cells[J]. Science Advances, 1(10): e1500372–e1500372.DOI:10.1126/sciadv.1500372 |
