 , 薛宇, 杨少林, 郑敏, 刘艳臣
, 薛宇, 杨少林, 郑敏, 刘艳臣
 , 黄霞
, 黄霞清华大学环境学院, 环境模拟与污染控制国家重点联合实验室, 北京 100084
收稿日期: 2017-12-25; 修回日期: 2018-02-19; 录用日期: 2018-02-19
基金项目: 国家自然科学基金(No.51678337);国家水体污染控制与治理科技重大专项(No.2014ZX07305001)
作者简介: 吴爽(1992-), 女, E-mail:1198370114@qq.com
通讯作者(责任作者): 刘艳臣, 副教授、博士生导师, 长期从事污水系统优化运行与管理的教学科研工作, 在国内外核心学术期刊上发表论文50余篇, 其中SCI收录30余篇.E-mail:liuyc@mail.tsinghua.edu.cn
摘要: 污水厂进水或厌氧单元出水中的硫化物会对污水处理工艺的硝化反应过程产生潜在抑制作用,认识和调控硫化物对活性污泥生化反应过程的影响对污水厂工艺的发展具有重要意义.亚硝化过程对于保障污水工艺氮的去除至关重要,本研究以硫化物对亚硝化过程的影响为研究对象,探讨相关影响过程的特征和发生机制.同时,选择不同典型浓度范围的硫化物和不同存在状态对亚硝化过程的影响开展研究.结果表明,硫化物浓度由10 mg·L-1提高到30 mg·L-1,氨氧化抑制率由16.3%提高到40%,但随着硫化物浓度进一步升高,氨氧化抑制率上升并不明显.进一步通过硫化物对羟胺氧化反应的影响实验发现,硫化物导致羟胺氧化速率下降要大于氨氧化阶段.同时系统内硫化物耗尽后,氨氧化反应和羟胺氧化反应均不能完全恢复.铁盐作为常见的硫化物去除剂,铁盐加入后并未能够有效消除硫化物对亚硝化过程的抑制.
关键词:硫化物亚硝化氨氧化抑制羟胺氧化抑制抑制恢复
Study on the inhibition of sulfide on activated sludge activity for nitritation
WU Shuang
 , XUE Yu, YANG Shaolin, ZHENG Min, LIU Yanchen
, XUE Yu, YANG Shaolin, ZHENG Min, LIU Yanchen
 , HUANG Xia
, HUANG Xia School of Environment, State Key Joint Laboratory of Environment Simulation and Pollution Control, Tsinghua University, Beijing 100084
Received 25 December 2017; received in revised from 19 February 2018; accepted 19 February 2018
Supported by the National Natural Science Foundation of China(No.51678337)and the Major Science and Technology Program for Water Pollution Control Treatment of China(No.2014ZX07305001)
Biography: WU Shuang (1992—), female, E-mail:1198370114@qq.com
*Corresponding author: LIU Yanchen, E-mail:liuyc@mail.tsinghua.edu.cn
Abstract: Understanding the impact of sulfide on the biochemical reaction of activated sludge for nitritation is great significance in wastewater treatment plants. This study systematically investigated the inhibition effect of sulfide on ammonia oxidation activity of activated sludge. The ammonia oxidation activity gradually decreased from 16.3% to 40%with the sulfide concentration increasing from 10 mg·L-1 to 30 mg·L-1, and maintained at this level despite that the sulfide concentration kept increasing. By the experiment of hydroxylamine oxidation rate, we found that sulfide inhibition effect on the hydroxylamine oxidation was bigger than ammonia oxidation. Afterwards, sulfide was aerobically depleted in the aqueous solution system. However, the ammonia and hydroxylamine oxidation activity could not both be recovered. Further experiment indicated that the ammonia oxidation activity could also not be recovered by adding ferrous chloride, which has been previously considered as a useful chemical for eliminating sulfide inhibition.
Keywords: sulfidenitritationammonia oxidation inhibitionhydroxylamine oxidation inhibitioninhibition recovery
1 引言(Introduction)污水处理过程中氮的去除至关重要, 目前常规途径主要通过硝化和反硝化过程实现污水中氨氮的去除(Wosiack et al., 2015), 在好氧条件下氨氮被氨氧化菌(Ammonia Oxidizing Bacteria, AOB)氧化为亚硝酸盐, 再被亚硝酸氧化菌(Nitrite Oxidizing Bacteria, NOB)氧化为硝酸盐, 其中, 氨氮被氧化为亚硝酸盐的过程被称为亚硝化过程(De la Torre-Velasco et al., 2013;Blackburne et al., 2007).亚硝化过程包括氨氮氧化作用和羟胺氧化作用, 氨氮在细胞膜上单胺氧化酶(Ammonia Monooxygenase, AMO)的作用下, 被氧气氧化为羟胺并释放到外周胞质, 羟胺在羟胺氧化酶的作用(Hydrolymine Oxidase, HAO)下失去电子, 生成NO2-并释放到细胞外(Ward et al., 2011):
 | (1) |
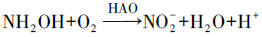 | (2) |
目前, 人们已开展了一些硫化物对硝化过程的研究, 例如, Ricardo等(2007)研究了流动生物膜反应器中的硝化细菌对硫化物的耐受力, 发现当S2-浓度为1.7 mg·L-1时对硝化细菌产生抑制, 当S2-浓度为13 mg·L-1时达到半抑制效应;Diego等研究了活性污泥中AOB对H2S的耐受力, 发现2.6 mg·L-1的硫化物将对AOB产生半抑制(Bejarano Ortiz et al., 2013);Sears等(2004)研究发现, 当S2-浓度为0.5 mg·L-1时氨氧化作用将被完全抑制.综上发现, 不同研究结果之间具有较大差异, 硫化物对硝化过程抑制影响依然不够清晰.
新型污水脱氮技术的开发与应用中, 短程硝化-反硝化(Ge et al., 2015;Cao et al., 2016;张小玲等, 2002)与短程硝化-厌氧氨氧化技术(Fernández et al., 2016;马斌, 2012;张树立, 2012)因高效的脱氮性能得到了越来越多的关注, 其中, 亚硝化过程的稳定控制是技术的关键(Sun et al., 2010).然而迄今为止有关硫化物对亚硝化富集污泥的抑制研究报道较少, 有关硫化物对亚硝化过程的抑制影响需要开展更加深入的研究, 相关工作对新型脱氮工艺调控也具有重要参考价值.
因此, 本研究以污水氨氮亚硝化过程为研究对象, 解析硫化物对氨氧化反应中氨氧化作用和羟胺氧化作用的抑制影响特征, 以期为不同工艺组合条件下氨氧化过程的稳定控制与实现提供技术支持, 并为解决实际污水处理过程中的硫化物抑制生物活性问题提供保障.
2 材料与方法(Materials and methods)2.1 亚硝化污泥富集实验所用污泥均为实验室驯化富集亚硝化污泥, 进水NH4+浓度为(1100±80) mg·L-1, NaHCO3为6 g·L-1, 通过控制碱度不足维持稳定的亚硝化效果. SBR反应器的有效容积为8 L, 处理水量8 L·d-1, 排空比为1/2, 高径比为2.5, 运行周期为12 h, 其中, 进水10 min, 曝气搅拌10 h, 沉淀40 min, 排水10 min, 静置1 h.同时保持DO≥4 mg·L-1, pH=7.0±0.3, 温度为(25±3) ℃.反应器内AOB活性很高, 出水NH4+的平均浓度为691 mg·L-1, 氨氮去除率保持在40%, 氨氮降解速率为25 mg ·L-1·h-1;出水中NO2-的平均浓度为444 mg·L-1, 亚硝酸盐积累率(以下简称NAR)为86%, 反应器内的NOB菌群无论是丰度还是活性均较低.SBR反应器中的氨氧化效果和NAR保持稳定, 污泥活性具备探究硫化物对亚硝化污泥抑制影响的实验条件.
2.2 硫化物抑制试验亚硝化是厌氧氨氧化和短程硝化反硝化脱氮工艺的关键技术, 而亚硝化过程包括氨氧化和羟胺氧化两个过程, 因此, 试验研究不同浓度硫化物对氨氧化作用和羟胺氧化作用的影响, 活性污泥取自2.1节中的SBR反应器, 反应器内污泥浓度(MLSS)为2050 mg·L-1.
2.2.1 硫化物抑制氨氧化作用试验取1.5 L污泥泥水混合物, 静置1 h沉淀浓缩, 倒去上清液后加入3 L营养液, 然后平均分装至0.5 L的小型曝气反应器, 营养液配方如下:1.146 g NH4Cl、1.2 g NaHCO3、0.2 g K2HPO4、1.8 g KH2PO4.分装后分别加入不同浓度的硫化钠溶液, 操作示意图如图 1所示, 试验过程采用曝气控制DO浓度在4.0 mg·L-1以上, 控制温度为(25±2) ℃, 其它试验条件详见表 1.每隔0.5 h取污泥混合液样品10 mL, 离心取上清液经0.45 μm膜过滤后分析NH4+-N、NO2--N和NO3--N.
图 1(Fig. 1)
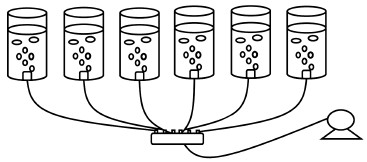 |
| 图 1 硫化物对氨氧化作用操作示意图 Fig. 1Schematic diagram of sulfide inhibiting ammoxidation experiment |
表 1(Table 1)
| 表 1 硫化物对氨氧化作用试验条件 Table 1 Experimental condition of sulfide inhibiting ammoxidation experiment | ||||||||||||||||||||||||||||||||
表 1 硫化物对氨氧化作用试验条件 Table 1 Experimental condition of sulfide inhibiting ammoxidation experiment
| ||||||||||||||||||||||||||||||||
2.2.2 硫化物抑制羟胺氧化作用试验取0.5 L污泥泥水混合物, 静置1 h沉淀浓缩, 倒去上清液后加入1 L营养液, 然后平均分装至0.5 L的小型曝气反应器, 营养液配方如下:50 μL 50%的NH2OH溶液、0.07 g K2HPO4、0.6 g KH2PO4.分装后分别加入不同浓度的硫化钠溶液, 试验条件详见表 2, 试验过程采用曝气控制DO浓度在4.0 mg·L-1以上, 控制温度为(25±2) ℃.每隔0.5 h取污泥混合液样品10 mL, 离心取上清液经0.45 μm膜过滤后分析NO2--N和NO3--N.
表 2(Table 2)
| 表 2 硫化物对羟胺氧化作用试验条件 Table 2 Experimental condition of sulfide inhibiting hydroxylamine oxidization experiment | ||||||||||||||||
表 2 硫化物对羟胺氧化作用试验条件 Table 2 Experimental condition of sulfide inhibiting hydroxylamine oxidization experiment
| ||||||||||||||||
2.3 Fe2+缓解抑制试验取0.5 L污泥泥水混合物, 静置1 h沉淀浓缩, 倒去上清液后加入1.5 L营养液, 然后平均分装至0.5 L的小型曝气反应器, 营养液配方如下:0.573 g NH4CL、0.6 g NaHCO3、0.1 g K2HPO4、0.9 g KH2PO4.分装后第2、3组分别加入16 mg·L-1的硫化钠溶液, 与此同时第3组加入等物质的量的FeCl2, 试验条件详见表 3, 试验过程采用曝气控制DO浓度在4.0 mg·L-1以上, 控制温度为(25±2) ℃.试验每隔0.5 h取污泥混合液样品10 mL, 离心取上清液经0.45 μm膜过滤后分析NH4+-N、NO2--N和NO3--N.
表 3(Table 3)
| 表 3 缓解抑制试验条件 Table 3 Experimental condition of relieving inhibition | |||||||||||||||||||||||||
表 3 缓解抑制试验条件 Table 3 Experimental condition of relieving inhibition
| |||||||||||||||||||||||||
2.4 仪器和检测方法分析仪器包括:溶解氧仪、ICS-2000型离子色谱(Dionex)、DR-5000紫外可见分光光度计(哈希)、氨氮微型测定仪(HI96700).
本实验所使用的化学试剂均为分析纯.进水和出水中的氨氮(NH4+-N)采用纳氏试剂分光光度法检测, 亚硝酸(NO2--N)采用盐酸萘乙二胺分光光度法检测, 硫化物(S2-)采用亚甲基蓝分光光度法检测, 硝酸根(NO3-)、硫代硫酸根(S2O32-)和硫酸根(SO42-)采用离子色谱仪(Dionex)检测.
3 结果与讨论(Results and discussion)3.1 硫化物对氨氧化过程的抑制作用图 2显示了投加不同浓度的硫化物后, 反应器内污泥氨氮降解速率的变化.从图 2可以看出, 随着硫化物投加浓度(以S计)的增加, 氨氮降解速率逐渐降低, 硫化物对氨氧化过程的抑制作用明显.加入10 mg·L-1硫化物后, 氨氮降解速率由9.2 mg·L-1·h-1下降为7.7 mg·L-1·h-1, 降低了16%, 硫化物投加浓度为30 mg·L-1时, 氨氮降解速率降低了40%.结果表明, 随着硫化物浓度的增高, 硫化物对氨氧化过程产生的抑制效应不断加强.然而硫化物浓度达到100 mg·L-1时, 氨氮降解速率降低比率依旧维持为40%, 这说明高浓度的硫化物并未进一步强化AOB代谢活性抑制.这个结果与其它已有研究结果有一定差异, 已有的关于CSTR反应器内AOB的硫化物半抑制浓度为0.5~2.6 mg·L-1(Sears et al., 2004;Bejarano Ortiz et al., 2013), 而生物膜反应器系统中硫化物对硝化细菌的半抑制浓度为13 mg·L-1(Blackburne et al., 2007).说明本研究体系内更加丰富的AOB菌群组成有效地提升了其对硫化物抑制作用的抵抗能力.
图 2(Fig. 2)
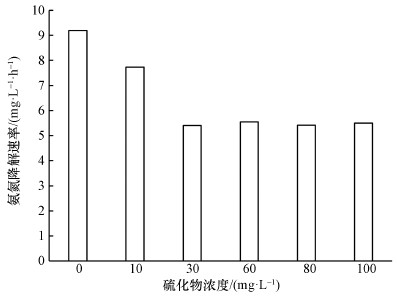 |
| 图 2 硫化物对NH4+降解速率的抑制影响 Fig. 2Inhibition of sulfide on ammonium oxidation |
同时, 从图 3中硫化物的变化情况可以看出, 反应体系内的硫化物在短时间内就会快速消失, 短时间内有大量的硫代硫酸盐作为中间氧化产物产生, 随后其又被快速氧化为硫酸盐, 但在这个过程中氨氮氧化速率仍受到显著的抑制影响, 并未能随着硫化物浓度降低而得到及时的恢复.这说明硫化物对氨氧化过程的抑制为微观瞬间酶抑制作用过程, 与反应过程中硫化物的持续暴露浓度无关, 仅受初始暴露硫化物浓度影响.
图 3(Fig. 3)
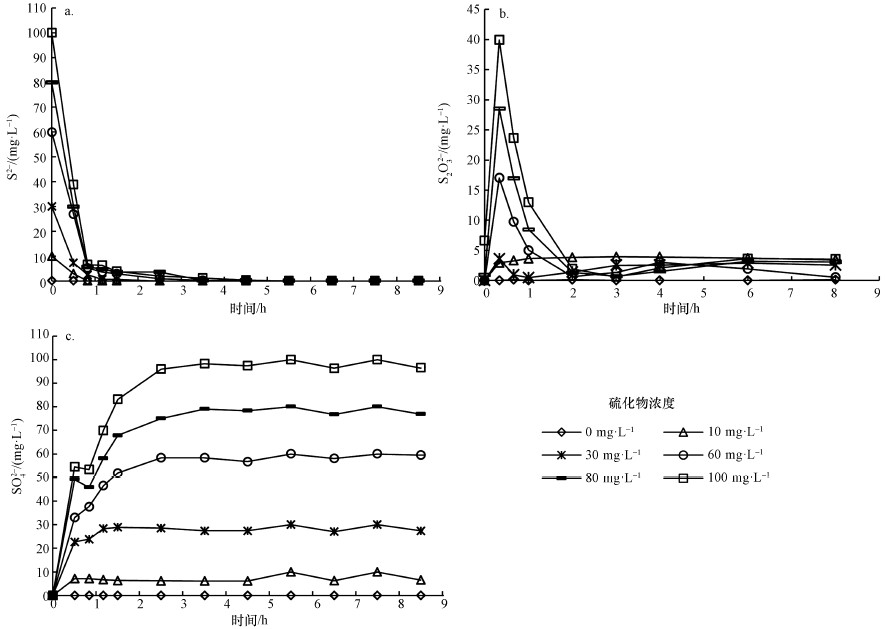 |
| 图 3 氨氧化过程中硫化物的变化(a.S2-, b.S2O32-, c.SO42-) Fig. 3Process of sulfide during ammonium oxidation |
氨单加氧酶(AMO酶)是参与AOB氧化氨氮为羟胺过程的主要膜蛋白酶, AMO和pMMO(particulate methane monooxygenase)具有极其相似的进化史, 根据pMMO晶体结构分析, 推测AMO具有α3β3γ3的亚基组成, 3个亚基分别是AmoA、AmoB、AmoC, 在亚基AmoA上存在催化氧化氨氮的含铜复合物活性位点, 因此, 推断硫化物穿过细胞周质空间与铜复合物结合, 形成同位不可逆的抑制作用, 从而对氨氧化过程产生影响, 而这个过程仅与AOB和硫化物的初始暴露浓度有关, 并且为不可逆抑制过程.
3.2 硫化物对羟胺氧化过程的抑制作用图 4a中显示了投加48 mg·L-1硫化物对羟胺氧化过程的影响结果, 可以看出, 对照组亚硝酸盐生成速率为0.73 mg·L-1·h-1, 而实验组(48 mg·L-1硫化物)亚硝酸的生成速率为0.22 mg·L-1·h-1, 同比下降了69%, 说明投加硫化物对羟胺氧化过程产生明显抑制作用.同时, 根据如上氨氧化过程硫化物抑制结果, 同样投加硫化物对氨氧化过程的抑制率为40%, 显著低于硫化物对羟胺氧化过程的抑制, 表明硫化物抑制氨氧化过程和羟胺氧化过程是同时发生的, 但硫化物对羟胺氧化过程抑制更加显著, 表现为限制性抑制作用.
图 4(Fig. 4)
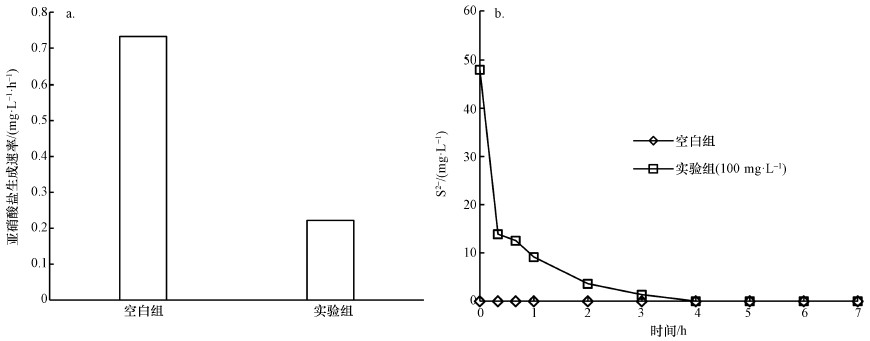 |
| 图 4 硫化物对羟胺过程中的影响(a.亚硝酸盐生成速率, b.硫化物浓度) Fig. 4Effect of sulfide on the hydroxylamine oxidation |
同样对比抑制发生过程硫化物浓度的时间变化(图 4b), 可发现反应体系内的硫化物在短时间内快速消失, 但实验组亚硝酸生成速率依旧受到显著抑制影响, 并且没有随着硫化物消失而得到及时恢复.羟胺氧化酶(HAO酶)是参与AOB氧化羟胺为NO2-过程的主要蛋白酶, 其中, 血红素P460是HAO酶的氧化活性位点, 硫化物可能与血红素P460上含铁卟啉结合形成较稳定的复合物, 使得P460不能与羟胺结合, 从而对羟胺氧化过程产生抑制影响, 同时抑制影响为不可恢复抑制作用.
3.3 硫化物抑制恢复研究二价铁盐与水中硫化物可以迅速生成硫化铁沉淀(Ahmad et al., 2016), 实验设计将Fe2+作为竞争S2-的抑制消除剂.从图 5a可以看出, 亚硝化混合污泥系统内只加入16 mg·L-1硫化物后, 硫化物被快速氧化耗尽, 同时氨氮降解速率下降了36.8%;而另外一组污泥同时加入等物质的量的硫化物与Fe2+, 反应立刻形成FeS黑色沉淀, 该组实验从始至终未检测到硫化物, 然而氨氮降解速率却下降了65.2%, 结果表明, 虽然Fe2+可以快速消除水中硫化物, 但却不能缓解或消除硫化物对亚硝化过程的抑制作用, 反而出现了抑制加剧现象.已有实验结果证明, Fe2+不会对氨氧化过程产生明显抑制作用(王秀蘅等, 2003).但通过对pH的研究发现, 当Na2S浓度为1 mmol·L-1时, 溶液的pH=10.0±0.1, 然而加入等物质的量的FeCL2后发现溶液的pH迅速从10.0下降为7.14, 因此, 溶液pH的迅速变化可能致使溶液中的H2S/HS-短时间内含量迅速增多, 从而强化了硫化物对亚硝化过程的抑制影响.
图 5(Fig. 5)
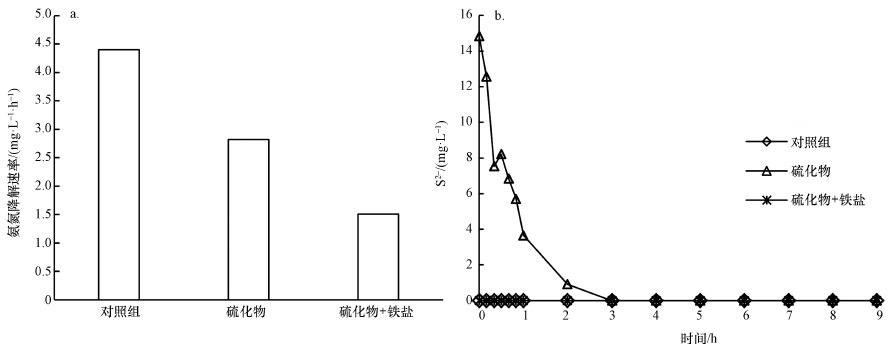 |
| 图 5 Fe2+缓解硫化物抑制结果(a.氨氮降解速率, b.硫化物浓度) Fig. 5Recovery of inhibition of sulfide on AOB by Fe2+ dosing |
4 结论(Conclusions)本文开展了硫化物对氨氮亚硝化过程影响的研究, 结果表明, 硫化物浓度由10 mg·L-1提高到30 mg·L-1时, 氨氧化抑制率由16%提高到40%, 表明浓度提高或能在一定程度上强化抑制效应, 然而污泥体系硫化物浓度继续增加到100 mg·L-1后, 氨氧化抑制率并未明显提高.污泥体系内加入48 mg·L-1硫化物后, 羟胺氧化速率降低69%, 说明硫化物对氨氧化过程和羟氨氧化过程均会产生明显的抑制作用, 硫化物对羟氨氧化过程抑制作用要强于其对氨氧化过程.二价铁盐作为去除溶液中硫化物的手段不能有效消除其对亚硝化过程的抑制影响, 溶液pH的降低将会进一步强化抑制影响.
参考文献
| Ahmad F, Maitra S, Ahmad N. 2016. Treatment of sulfidic wastewater using iron salts[J]. Arabian Journal for Science & Engineering, 42(4): 1–8. |
| Bejarano Ortiz D I, Thalasso F, Cuervo López F M, et al. 2013. Inhibitory effect of sulfide on the nitrifying respiratory process[J]. Journal of Chemical Technology and Biotechnology, 88(7): 1344–1349.DOI:10.1002/jctb.2013.88.issue-7 |
| Blackburne R, Vadivelu V M, Yuan Z, et al. 2007. Determination of growth rate and yield of nitrifying bacteria by measuring carbon dioxide uptake rate[J]. Water Environment Research, 79(12): 2437–2445.DOI:10.2175/106143007X212139 |
| Cao S B, Du R, Niu M, et al. 2016. Integrated anaerobic ammonium oxidization with partial denitrification process for advanced nitrogen removal from high-strength wastewater[J]. Bioresource Technology, 221: 31–46.DOI:10.1016/j.biortech.2016.09.019 |
| De la Torre-Velasco A, Beristain-Cardoso R, Damian-Matsumura P, et al. 2013. Sequential nitrification-denitrification process for nitrogenous, sulfurous and phenolic compounds removal in the same bioreactor[J]. Bioresource technology, 139: 220–225.DOI:10.1016/j.biortech.2013.03.190 |
| Fernández I, Dosta J, Mata-álvarez J. 2016. A critical review of the future trends and perspectives for the implementation of Anammox in the main line of municipal WWTPs[J]. Desalination and Water Treatment, 57: 27890–27898. |
| Ge S, Wang S, Yang X, et al. 2015. Detection of nitrifiers and evaluation of partial nitrification for wastewater treatment:A review[J]. Chemosphere, 140: 85–98.DOI:10.1016/j.chemosphere.2015.02.004 |
| Hu D X, Tian Y, Wang Z J, et al. 2017. The operational efficiency of a novel AnMBR treating antibiotic solvent wastewater in start-up stage[J]. Journal of Water Reuse and Desalination, 7(3): 326–337.DOI:10.2166/wrd.2016.064 |
| 蒋玲燕, 周振, 王英俊, 等. 2012. 硫化物对污水处理厂硝化菌活性的抑制作用[J]. 环境工程学报, 2012, 6(11): 4065–4068. |
| Krzeminski P, Leverette L, Malamis S, et al. 2017. Membrane bioreactors-a review on recent developments in energy reduction, fouling control, novel configurations, LCA and market prospects[J]. Journal of Membrane Science, 527: 207–227.DOI:10.1016/j.memsci.2016.12.010 |
| Liu Y, Wu C, Zhou X, et al. 2015. Effect of variation of liquid condition on transformation of sulfur and carbon in the sediment of sanitary sewer[J]. Journal of Environmental Management, 154: 65–69. |
| 马斌. 2012. 城市污水连续流短程硝化厌氧氨氧化脱氮工艺与技术[D]. 哈尔滨: 哈尔滨工业大学http://cdmd.cnki.com.cn/Article/CDMD-10213-1013035472.htm |
| Sears K, Alleman J E, Barnard J L, et al. 2004. Impacts of reduced sulfur components on active and resting ammonia oxidizers[J]. Journal of Industrial Microbiology & Biotechnology, 31(8): 369–378. |
| Song W, Li Z, Ding Y, et al. 2018. Performance of a novel hybrid membrane bioreactor for treating saline wastewater from mariculture:Assessment of pollutants removal and membrane filtration performance[J]. Chemical Engineering Journal, 331: 695–703.DOI:10.1016/j.cej.2017.09.032 |
| Sun S P, Nàcher C P, Merkey B, et al. 2010. Effective biological nitrogen removal treatment processes for domestic wastewaters with low C/N ratios:a review[J]. Environmental Engineering Science, 27(2): 111–126.DOI:10.1089/ees.2009.0100 |
| 王秀蘅, 任南琪, 王爱杰, 等. 2003. 铁锰离子对硝化反应的影响效应研究[J]. 哈尔滨工业大学学报, 2003, 35(1): 122–125.DOI:10.3321/j.issn:0367-6234.2003.01.030 |
| Ward B B, Arp D J, Klotz M G. 2011. Nitrification[M]. Washington, DC: American Society for Microbiology. 11-39 |
| Wosiack P A, Lopes D D, Damianovic M H R Z, et al. 2015. Removal of COD and nitrogen from animal food plant wastewater in an intermittently-aerated structured-bed reactor[J]. Journal of Environmental Management, 154: 145–150. |
| 张树立. 2012. 短程反硝化-厌氧氨氧化联合用于污水脱氮的研究[M]. 北京: 北京工业大学. |
| 张小玲, 彭党聪, 王志盈. 2002. 短程硝化-反硝化技术经济特性分析[J]. 西安建筑科技大学学报(自然科学版), 2002, 34(3): 239–242.DOI:10.3969/j.issn.1006-7930.2002.03.009 |
