通常将磁场强度低于5 μT的极弱磁场称为亚磁场(hypomagnetic field, HMF)。以往的研究发现亚磁场暴露会影响动物的认知过程,然而其背后的细胞分子机制尚不清楚。哺乳动物大脑的海马组织在动物的认知功能中发挥重要作用,在动物成年以后可持续产生新的功能性神经元,并整合到已有的神经环路中并参与学习和记忆等多种认知功能的调控(该过程称为成体海马神经发生)。成体海马神经发生受动物生理条件和环境因素的影响,地磁场作为地球生物生存的重要环境因子,其减弱对神经发生的影响研究将为评估包括人类在内的生物圈受亚磁场暴露的影响及应对策略提供重要科学依据;并且可为认识地磁场环境对动物中枢神经系统功能的作用提供有价值的参考。
中国科学院地质与地球物理研究所地球与行星物理院重点实验室地磁场与生物圈演化学科组博士研究生张兵芳与导师潘永信研究员、田兰香副研究员联合遗传与发育生物学研究所郭伟翔研究员等,采用多学科交叉研究方法,对长时间亚磁场暴露对C57BL/6J模式小鼠成体海马神经发生的影响开展系统性研究。基于亥姆霍兹线圈磁控系统和免疫荧光共定位技术分析发现:相比地磁场(GMF)组小鼠,亚磁场(HMF)连续暴露6周的小鼠,其海马齿状回区域神经干细胞的增殖和新生神经元的分化能力显著降低,新生神经元的树突总长度减少、分枝结构复杂度及突触棘密度显著降低。行为学分析发现,HMF组小鼠在海马功能依赖的新位置、新物体识别中均表现出明显的认知缺陷,表明连续6周以上的亚磁场暴露会减弱小鼠成体海马神经发生并影响其认知功能(图1)。
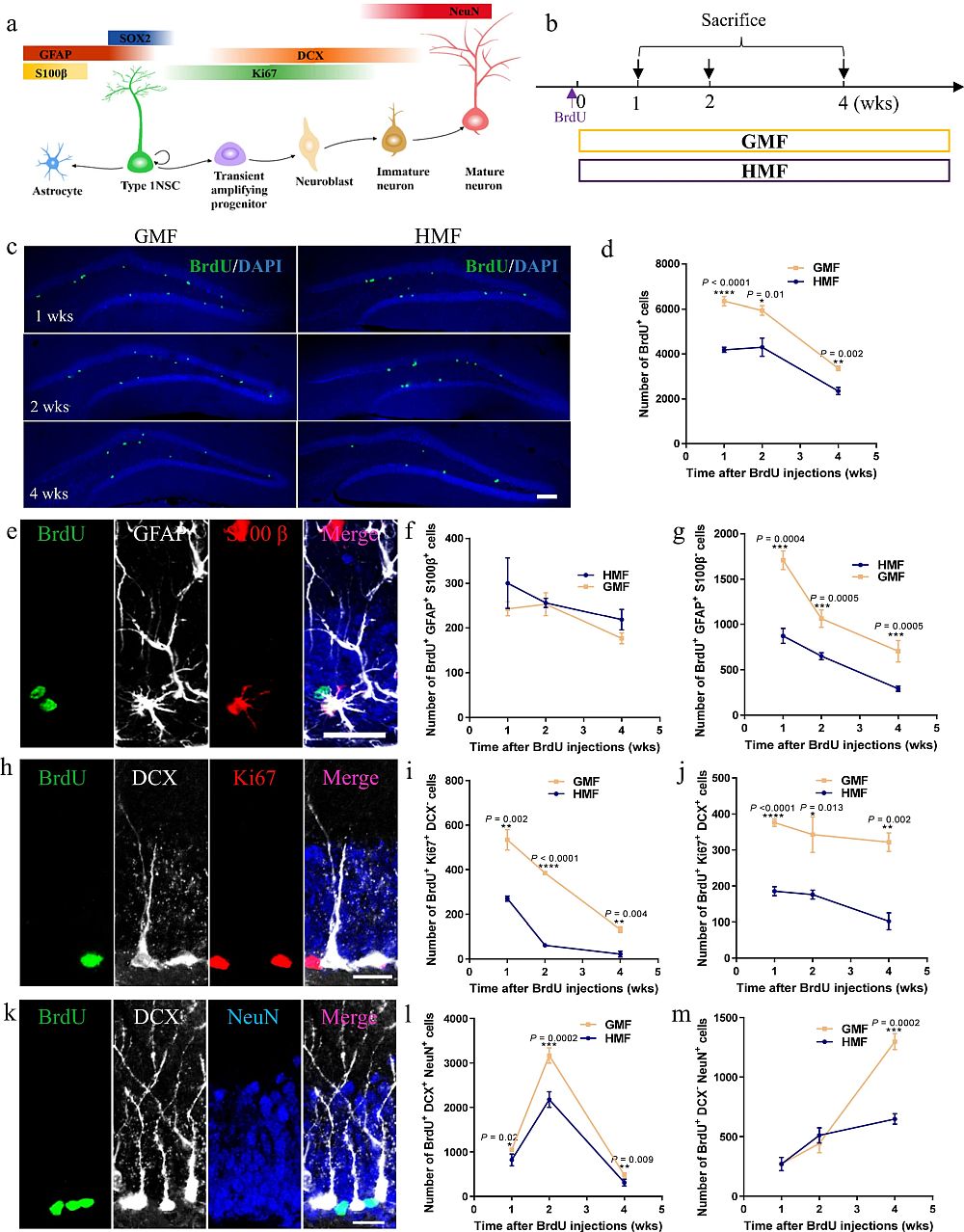
图1 亚磁场暴露减弱小鼠成体海马神经发生及海马依赖的认知行为。(a) 成体海马神经发生。 (b) 实验模拟的亚磁场和地磁场强度值。(c)成年小鼠经GMF- 和 HMF-暴露0-, 6-, 8-周后,海马齿状回(DG)区域增殖细胞(Ki67+)的免疫荧光照片。Scale bar = 100 μm。(d) GMF-和HMF-暴露小鼠海马DG区增殖细胞(Ki67+)数量统计结果。(e) 成体海马DG区新生的未成熟神经元(BrdU+DCX+NeuN+)和成熟神经元(BrdU+DCX-NeuN+)免疫荧光照片。Scale bar = 20 μm。(f) GMF-和HMF-暴露小鼠海马DG区新生未成熟神经元的数量统计图。(g) GMF-和HMF-暴露小鼠海马DG区新生的成熟神经元的数量统计图。(h) GMF-和HMF-暴露小鼠,DG区经逆转录病毒注射后RFP+新生神经元代表图。Scale bar = 50 μm。(i) GMF-和HMF-暴露小鼠,DG区逆转录病毒注射后RFP+新生神经元突触棘代表图。Scale bar = 10 μm。(j) GMF-和HMF-暴露小鼠对新旧位置识别差异的结果。(k) GMF-和HMF-暴露小鼠对新旧物体识别差异的结果
他们进一步研究了亚磁场对神经发生的影响是否可以通过返回地磁场环境获得恢复。研究发现相比GMF组小鼠,HMF暴露小鼠的神经干细胞ROS水平在将它们转移回GMF后可恢复到GMF暴露的对照水平。早在返回GMF后2周,海马齿状回区域神经干细胞的数量就显著增加,返回GMF后4周新生神经元的数量恢复到地磁场组水平,但星形胶质细胞的数量不受影响。新生神经元的树突长度和复杂性在返回GMF后4周显著恢复,在返回GMF后8周完全获救。行为学分析发现,通过返回GMF可以挽救暴露于HMF环境引起的海马依赖学习缺陷。因此,返回GMF能够改善由于长期暴露HMF环境引起的神经发生减弱和认知功能缺陷。
为理解亚磁场暴露影响小鼠成体海马神经发生及其认知功能的分子机制,他们从亚磁场暴露的成年Nestin-GFP转基因小鼠脑内分选出海马神经干细胞并进行转录组测序分析。结果显示,亚磁场处理显著升高了抑制干细胞增殖、分化相关基因的表达水平,同时降低了低氧应激、活性氧(reactive oxygen species, ROS)代谢和产生相关基因的表达水平。结合前人研究发现ROS可作为第二信使调控细胞信号通路以及磁场强度的变化会影响细胞内自由基浓度等认识,他们推断亚磁场可能通过降低海马神经干细胞内ROS的含量来影响成体海马神经发生。进一步ROS原位检测证实,亚磁场暴露显著降低了海马神经干细胞内的ROS水平(图2)。
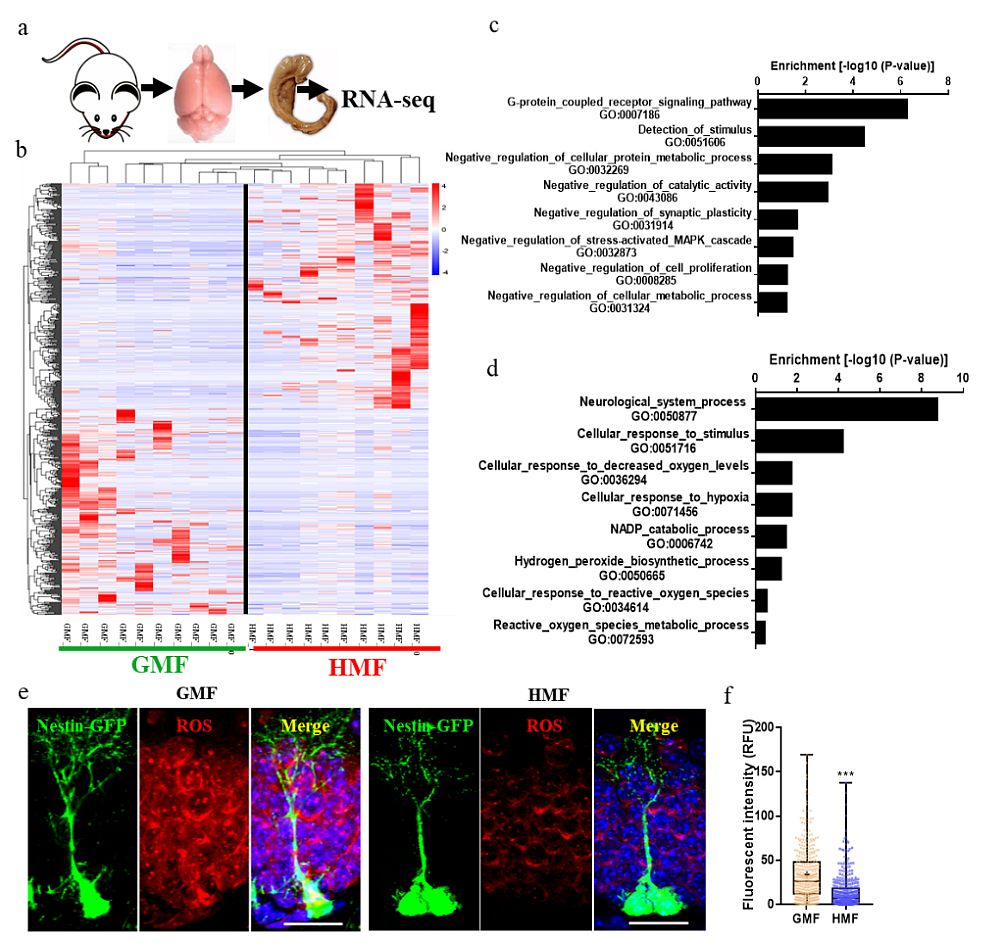
图2 亚磁场暴露降低小鼠成体海马神经干细胞内的ROS水平。(a)对成体海马神经干细胞进行转录组分析的研究策略。(b) GMF-和HMF-暴露的Nestin-GFP小鼠成体海马干细胞差异基因表达热图。(c 和 d) 差异表达基因的GO分析:显著上调基因的功能聚集 (c)和下调基因的功能聚集 (d)。(e) Nestin-GFP小鼠经GMF-和HMF-暴露8周后DG区神经干细胞内ROS原位检测图片。图中比例尺为20 μm。(f) Nestin-GFP小鼠经GMF-和HMF-暴露8周后DG区神经干细胞内ROS定量统计对比结果
通过注射超氧化物歧化酶(superoxide dismutase,SOD)酶活抑制剂二乙基二硫代氨基甲酸钠(DDC)提高海马干细胞内的ROS水平发现, DDC处理的亚磁场组小鼠海马神经干细胞的增殖和新生神经元的分化、树突发育及海马依赖的认知行为均恢复到地磁场组水平,这表明适当升高小鼠海马干细胞内的ROS水平可恢复亚磁场暴露对小鼠成体海马神经发生的损害。DDC处理的地磁场组小鼠海马神经干细胞ROS水平也升高,但是其增殖、神经元的分化和树突发育却受到明显抑制,且细胞的凋亡水平显著升高,这表明过高水平的ROS会损害小鼠成体海马神经发生(图3)。该结果证实亚磁场通过降低神经干细胞内的ROS影响小鼠成体海马神经发生,并且成体海马神经发生需要维持干细胞内适宜的ROS水平。
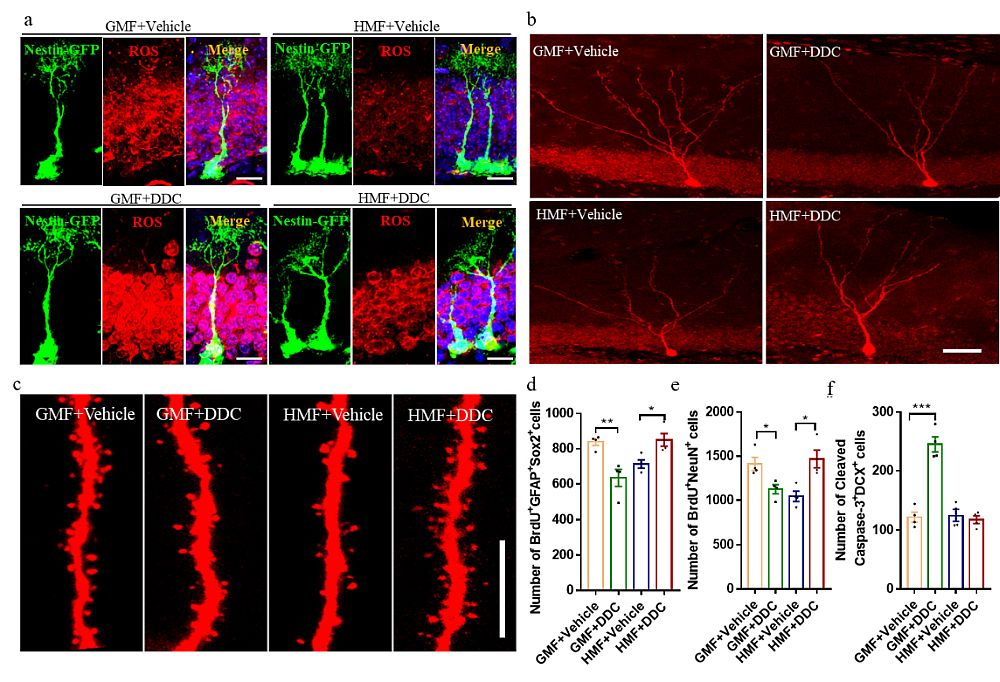
图3 升高ROS水平恢复亚磁场暴露小鼠成体海马神经发生。(a) GMF-和HMF-暴露的Nestin-GFP小鼠经DDC处理后,DG区神经干细胞内ROS原位检测示意图。Scale bar = 20 μm。(b) GMF-和HMF-暴露的小鼠经DDC处理后,DG区新生神经元树突结构示意图。Scale bar = 50 μm。 (c) GMF-和HMF-暴露的小鼠经DDC处理后,DG区神经新生神经元突触棘结构示意图。Scale bar = 10 μm。(d-f) GMF-和HMF-暴露的小鼠经DDC处理后,DG区BrdU+Sox2+GFAP+ 神经干细胞(d), BrdU+NeuN+神经元(e)及活性caspase-3+DCX+凋亡细胞的数量(f)
上述实验研究揭示ROS是磁场调控成体海马神经发生的重要因子,亚磁场通过降低细胞内ROS水平损害小鼠成体海马神经发生及认知功能(图4)。亚磁场暴露引起的神经发生和认知功能缺陷可以通过药物提高ROS水平或返回地磁场环境来挽救。本研究首次在动物水平上证实了地磁场/亚磁场、ROS与成体海马神经发生之间的关系,确认亚磁场的生物效应具有时间累积性,揭示出地磁场在小鼠成体海马神经发生中的重要性,同时为研究亚磁场的神经生物学效应机制提供了新的认识,为亚磁场生物效应的医学干预提供了参考策略。
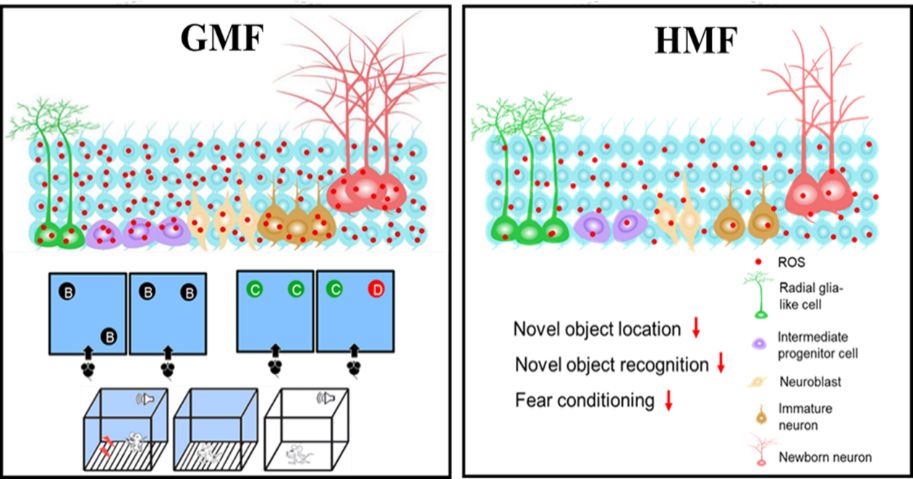
图4 GMF和HMF影响成体海马神经发生的作用机制。GMF通过维持细胞内适当高水平的ROS调控海马神经发生及海马依赖的认知,而亚磁场暴露降低了ROS水平进而损害成体海马神经发生及其依赖的认知
研究成果发表于国际顶级学术期刊Nature Communications。(张兵芳, Lei Wang, Aisheng Zhan, Min Wang, 田兰香*, 郭伟翔*, 潘永信. Long-term exposure to a hypomagnetic field attenuates adult hippocampal neurogenesis and cognition[J]. Nature Communications, 2021, 12: 1174. DOI: 10.1038/s41467-021-21468-x)。本研究得到国家自然科学基金委创新研究群体、中国科学院前沿科学重点研究计划等项目的资助。
